
【题目】食用醋中含有乙酸。下列关于乙酸的说法正确的是
A.结构简式为C2H4O2B.分子式为CH3COOH
C.分子中含有的官能团为羧基D.分子中原子之间只存在单键
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
【题目】一个完整的氧化还原反应方程式可以拆开,写成两个“半反应式”,一个是“氧化反应式”,一个是“还原反应式”。如Fe+Cu2+=Fe2++Cu,可拆写为氧化反应式:Fe-2e-=Fe2+,还原反应式:Cu2++2e-=Cu。据此,回答下列问题:
(1)将反应Zn+2H+=Zn2++H2↑拆写为两个“半反应式”:
氧化反应式:_______________________,还原反应式:_______________________。
(2)将反应2Fe3++Cu=2Fe2++Cu2+拆写为两个“半反应式”:
氧化反应式:_______________________,还原反应式:_______________________。
(3)已知某反应的两个“半反应式”为:氧化反应式CH4+10OH--8e-=![]() +7H2O,还原反应式O2+2H2O+4e-=4OH-,则氧化还原反应方程式为___________________。
+7H2O,还原反应式O2+2H2O+4e-=4OH-,则氧化还原反应方程式为___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】反应A(g)+B(g)C(g)+D(g)发生过程中的能量变化如图,△H 表示反应的焓变.下列说法正确的是( ) 
A.反应体系中加入催化剂,反应速率增大,E1减小,E2增大
B.反应体系中加入催化剂,反应速率增大,△H不变
C.△H<0,反应达到平衡时,升高温度,A的转化率增大
D.△H>0,反应达到平衡时,升高温度,A的转化率减少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学以反应2Fe3++2I﹣2Fe2++I2为原理,研究浓度对氧化还原性和平衡移动的影响.实验如图1: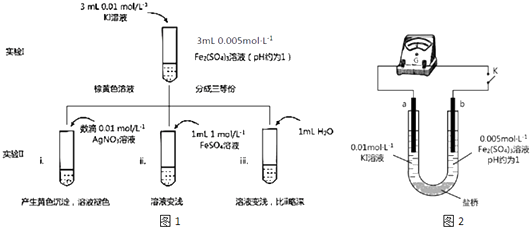
(1)待实验I溶液颜色不再改变时,再进行实验II,目的是使实验I的反应达到 .
(2)iii是ii的对比试验,目的是排除有ii中造成的影响.
(3)i和ii的颜色变化表明平衡逆向移动,Fe2+向Fe3+转化.用化学平衡移动原理解释原因: .
(4)根据氧化还原反应的规律,该同学推测i中Fe2+向Fe3+转化的原 因:外加Ag+使c(I﹣)降低,导致I﹣的还原性弱于Fe2+ , 用图2装置(a、b均为石墨电极)进行实验验证.①K闭合时,指针向右偏转,b作极.
②当指针归零(反应达到平衡)后,向U型管左管滴加0.01molL﹣1 AgNO3溶液,产生的现象证实了其推测,该现象是 .
(5)按照(4)的原理,该同学用右图装置进行实验,证实了ii中Fe2+向Fe3+转化的原因①转化原因是 .
②该实验与(4)实验对比,不同的操作是 .
(6)实验I中,还原性:I﹣>Fe2+;而实验II中,还原性:Fe2+>I﹣ , 将(3)和(4)、(5)作对比,得出的结论是 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的资源宝库。下图是从海水中提取食盐和溴的主要流程。

(1)粗盐除含 NaCl 外,还含有少量 MgCl2、 CaCl2、 Na2SO4以及泥沙等杂质。以下是粗盐提纯的
操作流程。

提供的试剂:
Na2CO3溶液、 K2CO3溶液、 NaOH 溶液、 BaCl2溶液、 Ba(NO3)2溶液、饱和 NaCl 溶液。
①除去溶液 I 中的 MgCl2、 CaCl2、 Na2SO4,从提供的试剂中选出 a 所代表的试剂,按滴加顺序依次为: 过量的NaOH 溶液、_______、_______;
②如何证明操作①中 NaOH 溶液已经过量?_______。
③蒸发过程所用的主要仪器有:铁架台、酒精灯、_______;
(2)某同学在实验室中用四氯化碳萃取较高浓度的溴水中的溴,经振荡并在铁架台上静置分层后,
①分离出四氯化碳层的操作是:_______。
②分离溴的四氯化碳溶液的操作方法是:_______。
(3)工业上将较高浓度的溴水经进一步处理得到工业溴。某研究性学习小组为了解从工业溴中提纯溴的方法,查阅了有关资料, Br2的沸点为 59℃,微溶于水,有毒性和强腐蚀性。水的沸点为 100℃。他们参观生产过程后,设计了如下装置简图:

①图中仪器 B 的名称:_______。
②用热水浴加热的优点是:_______。
③实验装置气密性良好,要达到提纯溴的目的,收集溴时温度计应控制的温度为:_______℃。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】精确配制一定物质的量浓度的溶液通常有两种方法:直接法和标定法。直接法是准确称量一定的物质,制成一定体积的溶液;标定法则是先粗略配制一定浓度的溶液,再用已知浓度的溶液标定其浓度。对于在空气中稳定,且试剂纯度高,组成和化学式相符的物质,通常采用直接法;而对于不易提纯、组成不定或容易分解的物质,则采用标定法。
(一)用无水碳酸钠固体配制250mL 0.1000mol/L碳酸钠溶液。
(1)计算需要碳酸钠固体的质量为ag,a=__________。
(2)用分析天平准备称量质量为ag的无水碳酸钠固体,为配制所需的碳酸钠溶液还需要的玻璃仪器有:________________________________________。
(二)用浓盐酸配制250mL约0.2mol/L盐酸并标定其精确浓度。
(3)计算需要浓盐酸(质量分数为36.5%,密度为1.2g/cm3)的体积为bmL,则b=__________(计算结果保留到小数点后一位)。
(4)用量筒量取bmL浓盐酸,缓慢加入盛有(250-b)mL水的烧杯中,用玻璃棒搅拌,即得所需溶液。
(5)用酸式滴定管(注:酸式滴定管是一种可较为精确量取液体体积的量器)量取25.00mL所配盐酸溶液,放入锥形瓶,逐滴加入上述碳酸钠溶液至正好完全反应生成NaCl溶液,消耗碳酸钠溶液的体积为25.00mL,则所配制盐酸的浓度为__________。
(6)为何不用直接法配制盐酸溶液?答:________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知碳碳单键可以绕键轴自由旋转,结构简式为: ![]() 的烃,下列说法正确的是( )
的烃,下列说法正确的是( )
A.分子中至少有9个碳原子处于同一平面上
B.分子中至少有11个碳原子处于同一平面上
C.分子中至少有16个碳原子处于同一平面上
D.该烃属于苯的同系物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列生活中常见物质的俗名与化学式相对应的是( )
A.生石灰﹣Ca(OH)2
B.小苏打﹣KHCO3
C.重晶石﹣CaSO4
D.醋酸﹣C2H4O2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com