
| A、9 | B、10 | C、11 | D、12 |
| 0.1mol/L×(V-x)L |
| (V+x)L |
| 9 |
| 11 |
| 9 |
| 11 |


 智慧小复习系列答案
智慧小复习系列答案科目:高中化学 来源: 题型:

| A、1 mol A最多能与4 mol H2发生加成反应 |
| B、有机物A可以在一定条件下与HBr发生反应 |
| C、有机物A与浓硫酸混合加热,可以发生消去反应 |
| D、1 mol A与足量的NaOH溶液反应,最多可以消耗 2 mol NaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
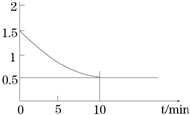 (1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;
(1)反应Fe(s)+CO2(g)?FeO(s)+CO(g)△H1,平衡常数为K1;| 700℃ | 900℃ | |
| K1 | 1.47 | 2.15 |
| K2 | 2.38 | 1.67 |
| c(CO) |
| c(CO2) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、负极的反应式为CH3OH+H2O-6e-═CO2↑+6H+ |
| B、电池的反应方程式是2CH3OH+3O2═2CO2+4H2O |
| C、电池工作时,H+由正极移向负极 |
| D、电池工作时,电子从通入甲醇的一极流出,经外电路再从通入氧气的一极流入 |
查看答案和解析>>
科目:高中化学 来源: 题型:
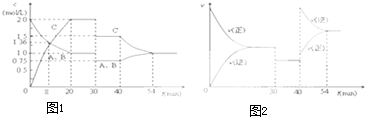
| A、第8min时 A的反应速率为0.08mol?L-1?min-1 |
| B、在0-54分钟的反应过程中该可逆反应的平衡常数始终为4 |
| C、30min时改变的条件是降低温度,40min时改变的条件是升高温度 |
| D、反应方程式中的x=1,且正反应为放热反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、H2、O3 |
| B、H2SO4、H2CO3 |
| C、SO2、NO |
| D、Na2SO3、KClO3 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com