
氯化硼的熔点为-107 ℃,沸点为12.5 ℃。在氯化硼分子中,氯—硼—氯键角为120°,它可以水解,下列对氯化硼的叙述,正确的是 ( )
A.氯化硼是原子晶体 B.熔化时,氯化硼能导电
C.氯化硼分子是一种极性分子 D.其水溶液显酸性
 培优口算题卡系列答案
培优口算题卡系列答案 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案科目:高中化学 来源: 题型:
X、Y、W、R、T是前17号元素中的5种,X、Y位于同主族,Y原子的最外层电子数与次外层电子数相等,R原子的最外层电子数为次外层电子数的3倍,T无正价,W单质用于制造计算机芯片,下列说法不正确的是( )
A.气态氢化物稳定性:W<T B.离子半径:X<R
C.最高价氧化物对应水化物碱性:X>Y D.Y单质能与冷水剧烈反应
查看答案和解析>>
科目:高中化学 来源: 题型:
某校化学课外小组为了鉴别碳酸钠和碳酸氢钠两种白色固体,用不同的方法做了以下实验,如图所示。
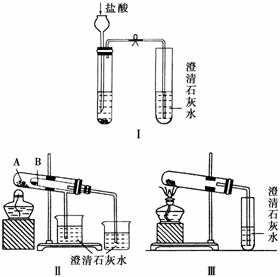
(1)只根据图Ⅰ所示实验,不能够达到实验目的的原因是
________________________________________________________________________。
(2)图Ⅱ、Ⅲ所示实验均能鉴别这两种物质,其反应的化学方程式为____________;
与实验Ⅲ相比,实验Ⅱ的优点是(填选项代号)________。
A.Ⅱ比Ⅲ复杂
B.Ⅱ比Ⅲ安全
C.Ⅱ比Ⅲ操作简便
D.Ⅱ可以做到用一套装置同时进行两个对比实验,而Ⅲ不行
(3)若用实验Ⅱ验证碳酸钠和碳酸氢钠的热稳定性,则试管B中装入的固体最好是(填化学式)________。
(4)将碳酸氢钠溶液与澄清石灰水混合并充分反应。
①当石灰水过量时,其离子方程式为_________________________________________。
②当碳酸氢钠与氢氧化钙物质的量之比为2∶1时,所得溶液中溶质的化学式为________,请设计实验检验所得溶液中溶质的阴离子__________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
在绿色化学工艺中,理想状态是反应物中原子全部转化为欲制得的产物,即原子利用率为100%。在用CH3C≡CH合成CH2===C(CH3)COOCH3的过程中,欲使原子利用率达到最高,还需要其他的反应物有( )
A.CO2和H2O B.CO和CH3OH
C.CH3OH和H2 D.H2和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
从海水中可提取下列物质:①H2O;②Mg;③NaCl;④K;⑤I2;⑥Br2。
(1) 请列举获取①的两种方法________、________。
(2)其中提取时可以不涉及化学变化的是_____,制取的单质在常温下是液体的是___。(填序号)
(3)从海水中提取镁可按如下步骤进行:①把贝壳制成石灰乳;②在引入的海水中加入石灰乳,沉降、洗涤、过滤沉淀物;③将沉淀物与盐酸反应,结晶、过滤、干燥产物;④电解得到产物。
以上提取镁的全过程中,没有涉及的化学反应类型是_____,进行①②③步骤的目的是_____,写出步骤④的化学方程式 。
查看答案和解析>>
科目:高中化学 来源: 题型:
短周期元素X、Y、Z,其中X、Y位于同一主族,Y、Z位于同一周期。X原子的最外层电子数是其电子层数的3倍,Z原子的核外电子数比Y原子少1。下列比较正确的是( )
A. 气态氢化物的稳定性:Z < Y < X B.最高价氧化物水化物酸性:Z > Y
C. 原子半径:Z < Y < X D. 元素非金属性:Z> Y > X
查看答案和解析>>
科目:高中化学 来源: 题型:
生物质能是一种洁净、可再生的能源。生物质气(主要成分为CO、CO2、H2等)与H2混合,催化合成甲醇是生物质能利用的方法之一。
(1)上述反应的催化剂含有Cu、Zn、Al等元素。写出基态Zn原子的核外电子排布式___________________________________________________________。
(2)根据等电子原理,写出CO分子的结构式_________________________。
(3)甲醇催化氧化可得到甲醛,甲醛与新制Cu(OH)2的碱性溶液反应生成Cu2O沉淀。
①甲醇的沸点比甲醛的高,其主要原因是________________________________;
甲醛分子中碳原子轨道的杂化类型为___________________。
②甲醛分子的空间构型是__________________;1 mol甲醛分子中σ键的数目为____________。
③在1个Cu2O晶胞中(结构如图所示),所包含的Cu+数目为__________。
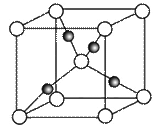
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式正确的是 ( )
A.实验室用大理石与醋酸反应制取二氧化碳:
CaCO3+2H+=Ca2++CO2↑+H2O
B.氯乙酸与氢氧化钠溶液共热: CH2ClCOOH+OH- →CH2ClCOO-+H2O
C.苯与浓硫酸、浓硝酸的混合液共热制硝基苯:
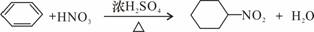
D.用银氨溶液检验乙醛中的醛基:
CH3CHO +2[Ag(NH3)2]++2OH-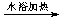 CH3COO-+NH4+ +3NH3+2Ag↓+ H2O
CH3COO-+NH4+ +3NH3+2Ag↓+ H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
请完成下列各题:
(1)前四周期元素中,基态原子中未成对电子数与其所在周期数相同的元素有________种。
(2)第ⅢA、ⅤA族元素组成的化合物GaN、GaP、GaAs等是人工合成的新型半导体材料,其晶体结构与单晶硅相似。Ga原子的电子排布式为________。
(3)CH4中共用电子对偏向C,SiH 4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为_______________________________________________。
4中共用电子对偏向H,则C、Si、H的电负性由大到小的顺序为_______________________________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com