
| 实验操作 | 预期现象与结论 |
| 步骤1:用滴管取一定量3mol·L-1H2SO4于试管中,加热煮沸数分钟除去溶于其中的氧气 |  |
| 步骤2:用药匙取少量样品于试管中,用滴管加入适量除去氧气的3mol·L-1H2SO4并加热,充分反应得A溶液 | 固体溶解,溶液颜色有变化 |
| 步骤3:取少许A溶液于试管中,滴加1—2滴20%KSCN溶液,振荡 | ① |
| 步骤4:另取少许A溶液于试管中,滴加1—2滴0.2mol·L-1KMnO4溶液,振荡 | ② |
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
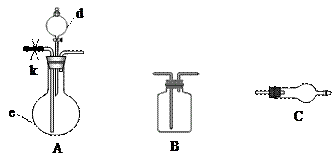
| 各装置连接次序 | | A | | | C | C |
| 对应的药品 | | d:浓盐酸 e:固体混合物 | | | 碱石灰 | 碱石灰 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
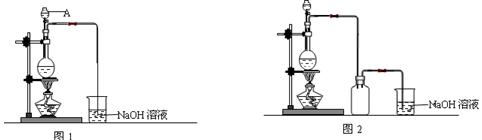
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.过滤 | B.蒸发 | C.分液 | D.萃取 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.石油分馏时把温度计插入液面下 |
| B.向银氨溶液中加入几滴乙醛后用酒精灯加热至沸制银镜 |
| C.在试管内加入少量蔗糖溶液,再加3-5mL稀硫酸小心煮沸几分钟后冷却,加入新制Cu(OH)2悬浊液,煮沸,有红色沉淀生成 |
| D.用乙醇、醋酸和18mol/L的硫酸混合加热制乙酸乙酯 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.只有①⑤⑥ | B.只有①③④⑤ | C.①②③④⑤ | D.只有③④⑤ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.在进行中和滴定是,先固定沉定管,后润洗、装液 |
| B.测定硫酸铜晶体的结晶水含量时,先称取一定量的晶体,后放入坩埚 |
| C.为检验酸性溶液中的Cl-和SO42-,先加硝酸银溶液,滤去沉淀后加硝酸钡溶液 |
| D.实验室抽取干燥纯净的氯气时,先使氯气通过饱和食盐水,后通过浓硫酸 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com