
| A. | B的阳离子的氧化性比A的阳离子强,则A元素的金属性不一定比B元素强 | |
| B. | 发生氧化还原反应时,A原子失去的电子比B原子多,证明A的金属性一定比B强 | |
| C. | 适量的Cl2通入FeI2溶液中可发生反应:3Cl2+6FeI2═2FeCl3+4FeI3 | |
| D. | A的金属性比B的金属性强,则A一定可以在水溶液置换出B来 |
分析 A.Fe3+的氧化性大于Cu2+的氧化性,而金属性Fe>Cu;
B.发生氧化还原反应时,由失去电子的难易可判断金属性,不能利用失去电子数目的多少来判断;
C.适量的Cl2通入FeI2溶液中,应先氧化碘离子;
D.如A与水反应,则不能置换出B.
解答 解:A.Fe3+的氧化性大于Cu2+的氧化性,而金属性Fe>Cu,故A正确;
B.发生氧化还原反应时,由失去电子的难易可判断金属性,不能利用失去电子数目的多少来判断,故B错误;
C.适量的Cl2通入FeI2溶液中,应先氧化碘离子,如加入过量氯气,则可生成氯化铁、碘,故C错误;
D.如A与水反应,则不能置换出B,如钠和硫酸铜溶液的反应,故D错误.
故选A.
点评 本题考查氧化性的比较,明确常见的氧化性比较的方法即可解答,注意A、C选项都是学生解答中的易错点,注意铁离子的氧化性较强,利用实例来说明问题.


 黄冈天天练口算题卡系列答案
黄冈天天练口算题卡系列答案科目:高中化学 来源: 题型:选择题
| A. | 常温下$\frac{c(O{H}^{-})}{c({H}^{+})}$=1012的溶液中:NH4+、Al3+、NO3-、CO32- | |
| B. | 滴加石蕊试剂显红色的溶液中:Na+、Fe2+、Cl-、NO3- | |
| C. | 常温下由水电离出来的c(H+)=1×10-13mol•L-1的溶液中:K+、CO32-、Cl-、NO3- | |
| D. | 常温下,$\frac{{K}_{W}}{c({H}^{+})}$=0.1 mol•L-1的溶液:Na+、K+、CO32-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
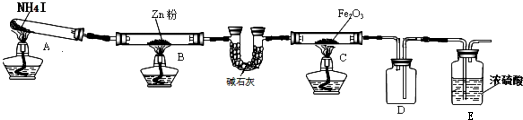
| 步骤 | 操作 | 甲组现象 | 乙组现象 |
| 1 | 取黑色粉末加入稀盐酸 | 溶解,无气泡 | 溶解,有气泡 |
| 2 | 取步骤1中溶液,滴加KSCN溶液 | 变红 | 无明显变化 |
| 3 | 向步骤2溶液中滴加新制氯水 | 红色先变深后褪去 | 先变红后也褪色 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 是配制一定物质的量浓度的溶液的专用仪器 | |
| B. | 容量瓶可以用来加热 | |
| C. | 能用容量瓶贮存配制好的溶液 | |
| D. | 可以用500mL容量瓶配制250mL溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
.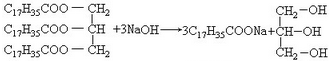 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
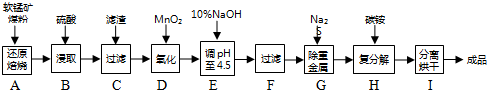
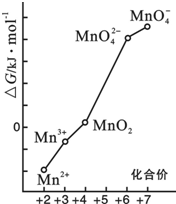
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CH3OH(g)+H2O(l)-6e-═CO2(g)+6H+(aq) | B. | CH3OH(g)+O2(g)-2e-═H2O(l)+CO2(g)+2H+(aq) | ||
| C. | O2(g)+4H+(aq)+4e-═2H2O(l) | D. | O2(g)+2H2O(l)+4e-═4OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子式为C3H8与C6H14的两种有机物一定互为同系物 | |
| B. | 同系物的化学性质相似,物理性质随碳原子数的递增呈现规律性变化 | |
| C. | 两个相邻同系物的相对分子质量数值一定相差14 | |
| D. | 分子组成相差一个或几个CH2原子团的化合物必定互为同系物 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com