
【题目】如图甲表示麦芽糖酶催化麦芽糖水解的模型,图乙表示在最适温度下,麦芽糖酶的催化速率与麦芽糖量的关系。

(1)该模型能解释酶的催化具有专一性,酶的专一性是指 __________ ,图中d和e代表 。
(2)限制g~h上升的原因是 ,如果温度升高5℃,g点将 (填“上移”或“不变”或“下移”),原因是 。
(3)能否用斐林试剂鉴定麦芽糖酶是否完成对麦芽糖的催化分解? (填“能”或“不能”)
(4)在3支试管中分别加入2mL 3%的可溶性淀粉溶液,并分别放到沸水、热水(约60℃)和冰块中;5min后,再在3支试管中分别加入1mL 2%的新鲜淀粉酶溶液,摇匀;5min后,又在3支试管中各滴入2滴碘液,摇匀并观察3支试管中溶液颜色的变化情况。请回答:
①该实验的目的是 。
②该实验的原理是 。
【答案】(1)一种酶只能对一种底物或一类底物起催化作用 葡萄糖
(2)酶的数量 下移 温度过高使酶的空间结构遭到破坏,活性降低
(3)不能
(4)① 探究不同温度对酶活性的影响(2分)
② 淀粉遇碘液变蓝,淀粉的水解产物遇碘液不变蓝(2分)
【解析】(1)酶的专一性是指一种酶只能催化一种或一类物质的化学反应;由以上分析可知,图中d和e代表葡萄糖。
(2)g~h段,随着麦芽糖浓度的升高,催化速率不变,原因是酶数量的限制;图乙是在最适温度下获得的曲线,如果温度升高5℃,使酶的空间结构遭到破坏,则酶活性将会降低,催化速率减慢,所以g点将下移。
(3)麦芽糖及麦芽糖水解形成的葡萄糖均为还原糖,因此不能用斐林试剂鉴定麦芽糖酶是否完成对麦芽糖的催化分解。
(4)①该实验的自变量是温度,因变量是酶的活性,因此其目的是探究温度为酶活性的影响。
②该实验的原理是淀粉遇碘变蓝色,淀粉酶催化淀粉水解,产物遇碘不变蓝色。


 课课优能力培优100分系列答案
课课优能力培优100分系列答案 优百分课时互动系列答案
优百分课时互动系列答案科目:高中化学 来源: 题型:
【题目】下图表示的是在最适温度下,反应物浓度对酶所催化的化学反应速率的影响,请分析回答:
(1)酶是活细胞产生的具有 作用的有机物,其本质绝大多数是 ,少数是 。
(2)随着反应物浓度的增加,反应速率加快,在 点达到最高值,限制反应速率增高的原因是。
(3)在A点适当提高反应温度,反应速率 ;在C点提高反应物浓度,反应速率 ,产物量 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】分析下列反应在任何温度下均能自发进行的是( )
A. 2N2(g)+O2(g)![]() 2N2O(g) ΔH=+163 kJ·mol-1
2N2O(g) ΔH=+163 kJ·mol-1
B. Ag(s)+ ![]() Cl2(g)
Cl2(g)![]() AgCl(s) ΔH=-127 kJ·mol-1
AgCl(s) ΔH=-127 kJ·mol-1
C. HgO(s)![]() Hg(l)+
Hg(l)+ ![]() O2(g) ΔH=+91 kJ·mol-1
O2(g) ΔH=+91 kJ·mol-1
D. H2O2(l)![]()
![]() O2(g)+H2O(l) ΔH=-98 kJ·mol-1
O2(g)+H2O(l) ΔH=-98 kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种气态烷烃X和一种气态烯烃Y组成的混合物10g,其密度为相同条件下氢气密度的12.5倍,该混合气体通过溴水,使溴水增重8.4g,则X、Y可能是( )
A. 甲烷和丙烯 B. 乙烷和乙烯 C. 甲烷和乙烯 D. 乙烯和丙烯
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组微粒的空间构型相同的是( )
①NH3和H2O ②NH4+和H3O+ ③NH3和H3O+ ④O3和SO2 ⑤CO2和C2H2 ⑥SiO44-和SO42-
A. 全部 B. 除①④⑥以外 C. ③④⑤⑥ D. ②⑤⑥
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应属于吸热反应的是
A. 氢氧化钠与盐酸反应 B. 葡萄糖与氧气反应
C. 氧化钙与水反应 D. Ba(OH)28H2O晶体与NH4Cl反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】运用化学反应原理研究氮、硫等单质及其化合物的反应有重要意义。
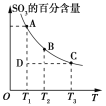
(1)硫酸生产过程中2SO2(g)+O2(g)![]() 2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图所示,根据如图回答下列问题:
2SO3(g),平衡混合体系中SO3的百分含量和温度的关系如图所示,根据如图回答下列问题:
①2SO2(g)+O2(g)![]() 2SO3(g)的ΔH________0(填“>”或“<”)。
2SO3(g)的ΔH________0(填“>”或“<”)。
②一定条件下,将SO2与O2以体积比为2︰1置于一体积不变的密闭容器中发生反应,能说明该反应已达到平衡的是________(填选项字母)。
a.体系的密度不发生变化
b.SO2与SO3的体积比保持不变
c.体系中硫元素的质量分数不再变化
d.单位时间内转移4 mol电子,同时消耗2 mol SO3
e.容器内的气体分子总数不再变化
(2)一定条件下,合成氨反应为:N2(g)+3H2(g)![]() 2NH3(g)。图1表示在此反应过程中的能量变化,图2表示在2 L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
2NH3(g)。图1表示在此反应过程中的能量变化,图2表示在2 L的密闭容器中反应时N2的物质的量随时间的变化曲线。图3表示在其他条件不变的情况下,改变起始物氢气的物质的量对此反应平衡的影响。
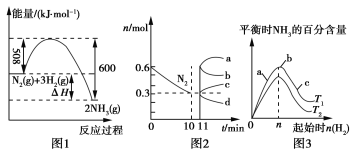
①该反应的平衡常数表达式为________,升高温度,平衡常数________(填“增大”“减小”或“不变”)。
②由图2信息,计算0~10 min内该反应的平均速率v(H2)________,从11 min起其他条件不变,压缩容器的体积为1 L,则n(N2)的变化曲线为________(填“a”“b”“c”或“d”)。
③图3a、b、c三点所处的平衡状态中,反应物N2的转化率最高的是________点,温度T1________T2(填“>”“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲、乙、丙三个容器中最初存在的物质及数量如图所示,三个容器最初的容积相等,温度相同,反应中甲、丙的容积不变,乙中的压强不变,在一定温度下反应达到平衡。下列说法正确的是
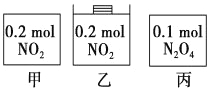
A. 平衡时各容器内c(NO2)的大小顺序为乙>甲>丙
B. 平衡时N2O4的百分含量:乙>甲=丙
C. 平衡时甲中NO2与丙中N2O4的转化率相同
D. 平衡时混合物的平均相对分子质量:甲>乙>丙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com