
 a、b、c、d均为短周期元素,它们在元素周期表中的位置关系如图所示,若b原子的最外层电子数是次外层电子数的3倍,下列说法中,正确的是( )
a、b、c、d均为短周期元素,它们在元素周期表中的位置关系如图所示,若b原子的最外层电子数是次外层电子数的3倍,下列说法中,正确的是( )| A、常见简单离子的半径:c>b>a |
| B、原子半径:c>d>b |
| C、最高价氧化物对应水化物的酸性:a>d |
| D、a的单质最稳定,不与任何物质发生化学反应 |


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、熔点:SiO2>NaCl>SiCl4 |
| B、稳定性:AsH3>PH3>NH3 |
| C、酸性:HClO4>H2SO4>H3PO4 |
| D、碱性:NaOH>Mg(OH)2>Al(OH)3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、只含有一种元素的物质一定是纯净物 |
| B、石墨转变为金刚石为化学变化 |
| C、水很稳定是因为水分子间存在较强的分子间作用力 |
| D、相对分子质量相同的不同物质一定是同分异构体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、分子中的中心原子通过SP2杂化轨道成键时,该分子一定为平面三角形 |
| B、CH4分子中有四个完全相同的sp3-s6键 |
| C、杂化轨道只用于形成6键 |
| D、杂化轨道理论与VSEPR模型分析分子的空间构型结果常常相互矛盾 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、(CH3)2CHCOOCH (CH3)2 |
| B、(CH3)2CHCOOCH(CH3)CH2CH3 |
| C、(CH3)2CHCOOCH2CH(CH3)2 |
| D、CH3(CH2)2COOCH2(CH2)2CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
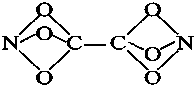 某学生利用C、N、O三种原子拼接成了一种新型分子TetranitiBtoxycarbon(结构如图所示),科学家经过研究发现,这种分子具有良好的贮能特性,一旦被合成完全可用于制造新的炸药.下列有关说法正确的是( )
某学生利用C、N、O三种原子拼接成了一种新型分子TetranitiBtoxycarbon(结构如图所示),科学家经过研究发现,这种分子具有良好的贮能特性,一旦被合成完全可用于制造新的炸药.下列有关说法正确的是( )| A、该分子的分子式为CNO3 |
| B、分子中既含极性键又含非极性键 |
| C、C、N的化合价分别为+4、+3 |
| D、该物质为高分子化合物 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、65 mL,0.52 g |
| B、70 mL,0.56 g |
| C、100 mL,0.52 g |
| D、100 mL,0.8 g |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com