
【题目】一定条件下,可逆反应X(g)+3Y(g)![]() 2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是
2Z(g),若X、Y、Z起始浓度分别为c1、c2、c3(均不为0),当达平衡时X、Y、Z的浓度分别为0.1mol/L,0.3mol/L,0.08mol/L,则下列判断不合理的是
A.c1:c2=1:3B.X、Y的转化率不相等
C.平衡时,Y和Z的生成速率之比为3:2D.c1的取值范围为0<c1<0.14mo/L
【答案】B
【解析】
试题分析:若反应向正反应进行到达平衡,X、Y的浓度最大,Z的浓度最小,假定完全反应,则:
根据方程式X(气)+3Y(气)2Z(气),
开始(mol/L):c1c2c3
变化(mol/L):0.040.120.08
平衡(mol/L):0.10.30.08
c1=0,14c2=0.42c3=0
若反应逆正反应进行到达平衡,X、Y的浓度最小,Z的浓度最大,假定完全反应,则:
根据方程式X(气)+3Y(气)2Z(气),
开始(mol/L):c1c2c3
变化(mol/L):0.10.30.2
平衡(mol/L):0.10.30.08
c1=0c2=0c3=0.28
由于为可逆反应,物质不能完全转化所以起始时浓度范围为0<c(X)<0.14,0<c(Y)<0.42,0<c(Z)<0.28;A.X和Y平衡浓度为1:3,变化的量为1;3,所以起始量为1:3,c1:c2=1:3,故A正确;B.X、Y的变化量之比和起始量之比相同,所以转化率相同,故B错误;C.平衡时,Y和Z的生成速率之比为化学方程式系数之比为3:2,故C正确;D.依据上述计算,c1的取值范围为0<c1<0.14molL-1,故D正确;故选B。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】某物质R完全燃烧的化学方程式为:2R+3O2 ![]() 2CO2 + 4H2O 有关该反应,有下列说法:
2CO2 + 4H2O 有关该反应,有下列说法:
①R一定含碳、氢两种元素,可能含有氧元素
②R中碳元素的质量分数是37.5 %
③6.4g R完全燃烧,转移1.2NA个电子
④R的摩尔质量为32
若6.4 g R完全燃烧生成8.8 g CO2,则正确的一组是
A.① ② B. ③④ C.②④ D. ②③
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于反应N2O4![]() 2NO2在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点)。下列说法正确的是
2NO2在温度一定时,平衡体系中NO2的体积分数V(NO2)%随压强的变化情况如图所示(实线上的任何一点为对应压强下的平衡点)。下列说法正确的是
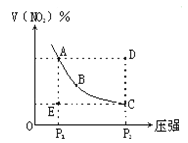
A、A、C两点的正反应速率的关系A>C
B、A、B、C、D、E各状态,V正>V逆的是状态D
C、使E状态从水平方向到达C状态,从理论上来讲,
可选用的条件是从P1突然加压至P2
D、维持P1不变,E→A所需时间为x,维持P2不变,D→C所需
时间为y,则x<y
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、D、E、F六种化合物,其中A、B、C、D、E均由短周期元素组成,焰色反应均为黄色,B、C、E均由三种元素组成。B、C的组成元素相同,且C的摩尔质量比B大80g/mol,回答:
(1)固体化合物A为浅黄色粉末,该化合物中含有的化学键为
A.离子键B.极性共价键C.非极性共价键D.氢键
(2)下表为B与F实验的部分内容
①在含B的溶液中加入稀H2SO4,产生浅黄色浑浊和使澄清石灰水变浑浊的无色有刺激性气味的气体 |
②20mL沸水中滴加F的饱和溶液1~2mL所得液体呈红褐色 |
③将实验②得到的红褐色液体加热蒸发,灼烧,最终得到红棕色固体 |
写出B与稀H2SO4反应的离子方程式
写出②中反应的化学方程式
(3).现由6种粒子Mn2+、MnO4-、H+、H2O、X2Y82-(C中含有的阴离子),XY42-完成一个离子方程式,已知Mn2+为还原剂,得到1molMnO4-需氧化剂的物质的量为mol
(4).化合物D和E相互转化D![]() E,若有D和E·
E,若有D和E·![]() H2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为g,E·
H2O的混合物13.04g,加热到完全反应后,气体产物通过浓H2SO4增重3.42g,剩余气体通过碱石灰增重2.20g,则混合物中D的质量为g,E·![]() H2O的化学式为
H2O的化学式为
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
A.0.1 mol·L-1(NH4)2Fe(SO4)2溶液中:c(SO![]() )=c(NH
)=c(NH![]() )>c(Fe2+)>c(H+)>c(OH-)
)>c(Fe2+)>c(H+)>c(OH-)
B.pH=2的HNO3溶液与pH=12的NH3·H2O溶液等体积混合:
c(NH![]() )+c(H+)=c(OH-)+c(NO
)+c(H+)=c(OH-)+c(NO![]() )
)
C.浓度均为0.1 mol/L的Na2CO3与NaHCO3混合溶液:
c(Na+)>c(HCO![]() )>c(CO
)>c(CO![]() )>c(OH-)
)>c(OH-)
D.0.1 mol/L NaHS溶液:c(OH-)=c(H+)+2c(H2S)+c(HS-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Cu与一定浓度的硝酸反应时,其方程式可表示为:
Cu+HNO3→Cu(NO3)2+NO↑+NO2↑+H2O
(1)硝酸在反应中体现了__________性和__________性;
(2)0.3 mol Cu被完全溶解后,如果得到的NO和NO2物质的量相同,则参加反应的硝酸的物质的量是多少?该NO和NO2混合气体的平均相对分子质量是多少?
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C是由周期表中短周期元素组成的三种常见化合物,甲、乙、丙是三种单质,这些单质和化合物之间存在如图1所示的关系,完成下列空白:

(1)向酚酞试液中加入化合物A的粉末,现象为_____________。
(2)单质甲与化合物B反应的离子方程式为_______________。
(3)向20mL某浓度的化合物C的溶液中通入CO2气体后得溶液M,因CO2通入量的不同,溶液M的组成也不同。若向M中逐滴加入0.1mol/L盐酸,产生的气体体积V(CO2)与加入盐酸的体积V(HCl)的关系如图2图示两种情况。

①由A确定滴加前60mL的盐酸时,发生反应的离子方程式为_________。
②由B表明,原溶液通入CO2气体后,所得溶液中的溶质的化学式为________。
③由A、B可知,两次实验通入的CO2的体积比为__________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com