
【题目】X、Y、Z、M、R为五种短周期元素,其原子半径和最外层电子数之间的关系如图所示。下列说法正确的是( )

A. 简单阳离子半径:X>R
B. X与Y可以形成正四面体结构的分子
C. M的氢化物常温常压下为液体
D. 最高价氧化物对应水化物的酸性:Z<Y
科目:高中化学 来源: 题型:
【题目】工业上,向500℃~600℃的铁屑中通入氯气生产无水氯化铁;向炽热铁屑中通入氯化氢气体生产无水氯化亚铁。现用如图所示的装置模拟上述过程进行试验。
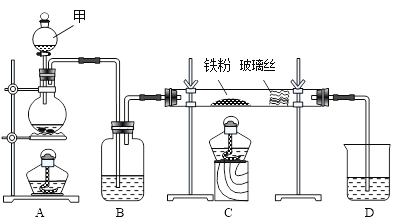
回答下列问题:
(1)制取无水氯化铁实验中,仪器甲的名称为_______________,进行实验时,应先点燃___________(选填A或C)处酒精灯。
(2)制取无水氯化铁的实验中,A中反应的离子方程式为_______________________,装置B中加入的试剂是____________________。
(3)制取的无水氯化铁中混有少量氯化亚铁,其原因是__________________(化学方程式表示)。为除去氯气中混有的少量HCl,可以在装置A、B间加入装有_______________的洗气瓶。
(4)工业上常用石灰乳吸收制氯气的尾气制得漂白粉,漂白粉的有效成分是_____________(填化学式)。长期露置于空气中的漂白粉,加稀盐酸后产生的气体是_____________(填数字代号)。
① O2 ② Cl2 ③ CO2 ④ HClO
(5)制取无水氯化亚铁实验中,装置A用来制取HCl气体,其化学方程式为:NaCl +H2SO4 (浓) ![]() NaHSO4+ HCl↑,通过装置C后尾气的成分是_________________。若仍用D的装置进行尾气处理,存在的主要问题是_________________________________________。
NaHSO4+ HCl↑,通过装置C后尾气的成分是_________________。若仍用D的装置进行尾气处理,存在的主要问题是_________________________________________。
(6)制取无水氯化亚铁实验中,若操作不当,制得的FeCl2会含有少量FeCl3,检验FeCl3常用的试剂是________________。(填化学式)欲制得纯净的FeCl2,在实验操作中应先__________________________,再___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某铁的“氧化物”样品,用5mol/L盐酸0.14L恰好完全反应,所得溶液还能吸收标准状况下2.24L氯气,使其中Fe2+全部转化为Fe3+.该样品可能的化学式是( )
A. Fe5O6 B. Fe3O4 C. Fe6O7 D. Fe5O7
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】水泥是重要的建筑材料.水泥熟料的主要成分为![]() 、
、![]() ,并含有一定量的铁、铝和镁等金属的氧化物.实验室测定水泥样品中钙含量的过程如图所示:
,并含有一定量的铁、铝和镁等金属的氧化物.实验室测定水泥样品中钙含量的过程如图所示:
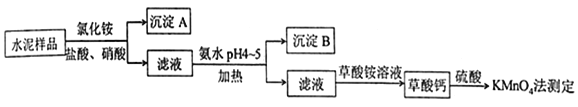
回答下列问题:
(1)在分解水泥样品过程中,以盐酸为溶剂,氯化铵为助溶剂,还需加入几滴硝酸.加入硝酸的目的是________,还可使用________代替硝酸.
(2)沉淀![]() 的主要成分是________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为_____________________________________________
的主要成分是________,其不溶于强酸但可与一种弱酸反应,该反应的化学方程式为_____________________________________________
(3)加氨水过程中加热的目的是__________________.沉淀![]() 的主要成分为________、________(填化学式).
的主要成分为________、________(填化学式).
(4)草酸钙沉淀经稀![]() 处理后,用
处理后,用![]() 标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为:
标准溶液滴定,通过测定草酸的量可间接获知钙的含量,滴定反应为: ![]() .实验中称取
.实验中称取![]() 水泥样品,滴定时消耗了
水泥样品,滴定时消耗了![]() 的
的![]() 溶液
溶液![]() ,则该水泥样品中钙的质量分数为________.
,则该水泥样品中钙的质量分数为________.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是镁的主要来源之一.从海水中提取镁可按如下步骤进行:①把贝壳制成石灰乳;②向引入的海水中加入石灰乳,沉降、洗涤、过滤沉淀物;③将沉淀物与盐酸反应,结晶、过滤、干燥;④电解得到产物.
(1)以上提取镁的全过程中,没有涉及的化学反应类型是(填序号).
A.分解反应
B.化合反应
C.置换反应
D.复分解反应
(2)下列关于提取镁的说法中不正确的是(填序号).
A.此法的优点之一是原料来自大海
B.进行①②③步骤的目的是富集MgCl2
C.可用电解熔融氧化镁的方法制取镁
D.电解冶炼镁要消耗大量电能
(3)电解熔融氧化镁制取镁的化学反应方程式 .
(4)③中沉淀物与盐酸反应的离子反应方程式 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】1,2-二溴乙烷可作抗爆剂的添加剂。如图为实验室制备1,2-二溴乙烷的装罝图, 图中分液漏斗和烧瓶a中分别装有浓H2SO4和无水乙醇,d装罝试管中装有液溴。
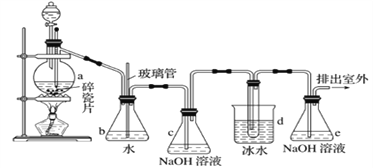
已知:Ⅰ.CH3CH2OH![]() CH2=CH2↑+H2O;2CH3CH2OH
CH2=CH2↑+H2O;2CH3CH2OH![]() CH3CH2OCH2CH3(乙醚)+H2O
CH3CH2OCH2CH3(乙醚)+H2O
Ⅱ.相关数据列表如下:
乙醇 | 1,2-二溴乙烷 | 乙醚 | 溴 | |
状态 | 无色液体 | 无色液体 | 无色液体 | 红棕色液体 |
密度/g·cm-3 | 0.79 | 2.18 | 0.71 | 3.10 |
沸点/℃ | 78.5 | 131.4 | 34.6 | 58.8 |
熔点/℃ | -114.3 | 9.79 | - 116.2 | -7.2 |
水溶性 | 混溶 | 难溶 | 微溶 | 可溶 |
(1)已知条件Ⅰ中有两个反应,其中第二个反应所属反应类型为____________________。
(2)实验中应迅速将温度升高到170℃左右的原因是______________________________。
(3)安全瓶b在实验中有多重作用。其一可以检查实验进行中d装罝中导管是否发生堵塞,请写出发生堵塞时瓶b中的现象:_______________________________;如果实验时d装罝中导管堵塞,你认为可能的原因是_______________________________________________;安全瓶b还可以起到的作用是__________________
(4)容器c、e中都盛有NaOH溶液,c中NaOH溶液的作用是________________________________。
(5)除去产物中少量未反应的Br2后,还含有的主要杂质为___________,要进一步提纯,下列操作中必需的是_____________ (填字母)。
A.重结晶 B.过滤 C.蒸馏 D.萃取
(6)实验中也可以撤去d装罝中盛冰水的烧杯,改为将冷水直接加入到d装罝的试管中,则此时冷水除了能起到冷却1,2-二溴乙烷的作用外,还可以起到的作用是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ⅰ.阅读短文,回答问题:
2017年7月9日,我国南海可燃冰试采工程全面完成预期目标,第一口井的试开采产气和现场测试研究工作取得圆满成功。自5月10日试气点火以来,取得了多项重大突破性成果,创造了产气时长和总量的世界纪录。可燃冰按其物质成分和结构特征来看,可称为天然气水合物,其形成条件主要包括物源条件和温压条件:物源条件要求有大量的天然气(主要是甲烷气)和水,它们是可燃冰形成的物质基础,没有它们将是“无米之炊”;环境条件则要求低温和高压,一般需要低于10℃的温度和大于100个大气压的压力(水深1000米以下),缺少这个条件“生米就不能煮成熟饭”。
请依据以上短文,判断下列说法是否正确(填“对”或“错”)。
(1)天然气燃烧是放热反应。______
(2)天然气是可再生能源。______
(3)可燃冰形成的环境条件是低温和高压。______
Ⅱ. 已知乙烯能发生以下转化:
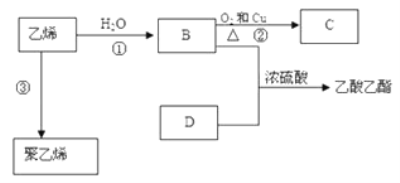
(4)乙烯的结构式为:___________________ 。
(5)B中所含官能团的化学式为____________________,其名称为____________________。
(6)写出下列反应的化学方程式并注明反应类型:
②___________________________________________________,反应类型____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com