
请回答下列问题:
(1)从以下仪器中选出本实验不需要使用的仪器(用字母填写)_______________。
A.托盘天平 B.研钵 C.试管夹 D.酒精灯 E.蒸发皿 F.玻璃棒 G.坩埚 H.干燥器 I.泥三角 J.石棉网 K.三脚架 L.药匙 M.坩埚钳
(2)该实验中哪一步骤需要使用干燥器?使用干燥器的目的是什么?
答:___________________________________。
(3)做此实验,至少应进行称量操作_______________次,至少加热_______________次。
(4)实验步骤⑥的目的是_____________________________________________。
(5)实验后得到以下数据:
①加热前质量:W1(容器),W2(容器+晶体);②加热后质量:W3(容器+无水硫酸铜)。
请写出硫酸铜晶体中结晶水含量,用质量分数表示的计算式(含W1、W2、W3)为:_____________。
(6)若操作正确但实验测得的硫酸铜晶体中结晶水的含量偏低,其原因可能有____________。
A.被测样品中含有加热不挥发的杂质
B.被测样品中含有加热易挥发的杂质
C.实验前被测样品已有部分失水
D.加热前所用的坩埚未完全干燥
解析:题目要求测定硫酸铜晶体中结晶水的含量,关键是要测定出一定质量的硫酸铜晶体中结晶水的质量。然后用下式求算:
结晶水的含量=![]() ×100%。
×100%。
所以,凡是能引起m(H2O)减小的操作都能使测量结果偏低。(6)中A、C两种情况下测量结果肯定偏低,B、D两种情况则会使结果偏高。
m(H2O)是实验前后固体质量差,因此每次实验操作就必须考虑到操作的精确性。实验步骤⑥的目的就是检验样品中的结晶水是否已经全部失去。
从题目信息我们不难看出,m(H2O)=W2-W3,m(硫酸铜晶体)=W2-W1。则:
样品中结晶水的含量为:![]() ×100%。
×100%。
答案:(1)CEJ
(2)冷却(或④);防止吸水
(3)4 2
(4)检验样品中的结晶水是否已经全部失去
(5)![]() ×100%
×100%
(6)AC


科目:高中化学 来源: 题型:阅读理解
| 沉淀物 | Fe(OH)2 | Fe(OH)3 | Al(OH)3 | Cu(OH)2 |
| 开始沉淀 | 5.8 | 1.1 | 4.0 | 5.4 |
| 完全沉淀 | 8.8 | 3.2 | 5.2 | 6.7 |
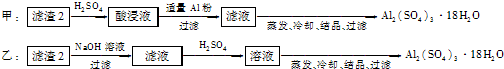
2- 3 |
2- 6 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
①能用于干燥二氧化硫气体的装置有__________(填字母)。
②装置B除可用于制取CO2、H2,还可制取__________、__________。(写出两种物质的化学式)
③既能用于收集氯气又能用于收集一氧化氮气体的装置有__________。(填字母)

(2)下列实验操作或实验事实的叙述不正确的是_____________(填序号)。
A.过滤、蒸发操作过程中都需要用玻璃棒不断搅拌液体
B.在试管中放入几片碎滤纸片,加入几滴90%的浓硫酸,捣成糊状,微热并冷却后,先滴入几滴CuSO4溶液,再加入过量的NaOH溶液中和至出现Cu(OH)2沉淀。加热至沸腾,可观察到红色沉淀生成
C.制备硫酸亚铁晶体时,向废铁屑中加入过量稀硫酸,充分反应后,过滤,然后加热蒸干滤液即可得硫酸亚铁晶体
D.测定硫酸铜晶体结晶水含量的实验中,称量操作至少要进行4次
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下列四种实验装置(根据需要可在其中加入液体或固体):
①能用于干燥二氧化硫气体的装置有__________(填字母)。
②装置B除可用于制取CO2、H2,还可制取__________、__________。(写出两种物质的化学式)
③既能用于收集氯气又能用于收集一氧化氮气体的装置有__________。(填字母)

(2)下列实验操作或实验事实的叙述不正确的是_____________(填序号)。
A.过滤、蒸发操作过程中都需要用玻璃棒不断搅拌液体
B.在试管中放入几片碎滤纸片,加入几滴90%的浓硫酸,捣成糊状,微热并冷却后,先滴入几滴CuSO4溶液,再加入过量的NaOH溶液中和至出现Cu(OH)2沉淀。加热至沸腾,可观察到红色沉淀生成
C.制备硫酸亚铁晶体时,向废铁屑中加入过量稀硫酸,充分反应后,过滤,然后加热蒸干滤液即可得硫酸亚铁晶体
D.测定硫酸铜晶体结晶水含量的实验中,称量操作至少要进行4次
查看答案和解析>>
科目:高中化学 来源:2012-2013学年江苏省无锡市高三上学期期末考试化学试卷(解析版) 题型:实验题
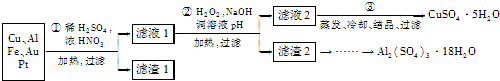
信息时代产生的大量电子垃圾对环境构成了极大的威胁。某化学兴趣小组将一批废弃的线路板简单处理后,得到主要含Cu、Al及少量Fc、Au、Pt等金属的混合物,设计了如下制备硫酸铜晶体和硫酸铝晶体的路线:

部分阳离子以氢氧化物形式沉淀时溶液的pH见下表
|
沉淀物 |
Fe( OH)2 |
Fe( OH)3 |
Al( OH)3 |
Cu( OH)2 |
|
开始沉淀 |
5.8 |
1.1 |
4.0 |
5.4 |
|
完全沉淀 |
8.8 |
3.2 |
5.2 |
6.7 |
请回答下列问题:
(1)第①步操作前需将金属混合物进行粉碎,其目的是 ;
(2)某学生认为用H2O2代替浓HNO3更好,理由是 ;
请写出Cu溶于H2O2与稀硫酸混合溶液的离子方程式是 。
(3)第②步中应将溶液pH调至 。
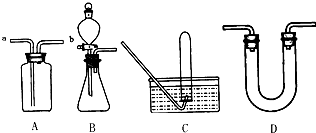
(4)由滤渣2制取Al2( SO4)3.18H2O,探究小组设计了两种方案:

你认为 种方案为最佳方案,理由是 、 。
(5)为了测定硫酸铜晶体的纯度,某同学准确称取4.0g样品溶于水配成l00mL溶液,取l0m溶液于带塞锥形瓶中,加适量水稀释,调节溶液pH=3~4,加入过量的KI,用0.l000mol·L-1Na2S2O3标准溶液滴定至终点,共消耗14. 00mL Na2S2O3标准溶液。上述过程中反应的离子方程式如下:
2Cu2+ +4I-=2CuI(白色)↓+I2
2S2O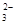 +I2=
2I-+S4O
+I2=
2I-+S4O
①样品中硫酸铜晶体的质量分数为____ 。
②另一位同学提出通过测定样品中硫酸根离子的量也可求得硫酸铜晶体的纯度,其他同学认为此方案不可行,理由是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com