
分析 水的电离是吸热反应,升高温度促进水电离,导致水的离子积常数增大;
pH=1的硫酸溶液中c(H+)=0.1mol/L,pH=10的NaOH溶液中c(OH-)=$\frac{1{0}^{-12}}{1{0}^{-10}}$mol/L=0.01mol/L,混合溶液呈中性,说明酸中n(H+)等于碱中n(OH-);
若混合溶液pH=2,则混合溶液中c(H+)=0.01mol/L=$\frac{0.1mol/L×bL-0.01mol/L×aL}{(a+b)L}$.
解答 解:水的电离是吸热反应,升高温度促进水电离,导致水的离子积常数增大,某温度时,水的离子积常数KW=10-12>10-15,说明该温度大于25℃;
pH=1的硫酸溶液中c(H+)=0.1mol/L,pH=10的NaOH溶液中c(OH-)=$\frac{1{0}^{-12}}{1{0}^{-10}}$mol/L=0.01mol/L,混合溶液呈中性,说明酸中n(H+)等于碱中n(OH-),所以0.1b=0.01a,a:b=10:1;
若混合溶液pH=2,则混合溶液中c(H+)=0.01mol/L=$\frac{0.1mol/L×bL-0.01mol/L×aL}{(a+b)L}$,a:b=9:2,
故答案为:大于;10:1;9:2.
点评 本题以酸碱混合溶液大小判断为载体考查pH的计算,为高频考点,侧重考查学生分析计算能力,把握溶液的pH值与氢离子或氢氧根离子浓度关系是解本题关键,知道混合溶液pH的计算方法,题目难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
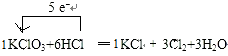 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题

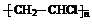 ,GHOOC(CH2)4COOH.
,GHOOC(CH2)4COOH.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 实验剩余的药品不能放回原瓶 | B. | 在实验前进行实验装置气密性检查 | ||
| C. | 可燃性气体的验纯 | D. | 胶头滴管不能交叉使用 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 62gNa2O溶于水后所得溶液中含有的O2-数为NA | |
| B. | 46gNO2和46gN2O4中含有的原子数均为3NA | |
| C. | 标准状况下,33.6L氟化氢中含有的氟原子数为1.5NA | |
| D. | 50mL18.4mol•L-1浓硫酸与足量铜微热反应,生成SO2的分子数为0.46NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题

| A. | 按系统命名法命名,图1化合物的名称是2,4,6一三甲基-5-乙基庚烷 | |
| B. | 图2有机物的一种芳香族同分异构体能发生银镜反应 | |
| C. | 图2有机物能使酸性高锰酸钾溶液褪色 | |
| D. | 图3为髙分子化合物,其单体为对苯二甲酸和乙二醇 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com