
【题目】在恒温下的密闭容器中,有可逆反应![]() ,下列不能说明该反应已达到平衡状态的是( )
,下列不能说明该反应已达到平衡状态的是( )
A.正反应生成NO2的速率和逆反应生成O2的速率
B.混合气体的颜色不再改变
C.反应容器中的压强不随时间的变化而变化
D.混合气体的平均摩尔质量保持不变
【答案】A
【解析】
A.正反应生成NO2的速率和逆反应生成O2的速率之比等于2:1时,反应达到平衡状态,符合题意,A正确;
B.NO为无色,NO2为红棕色,当混合气体的颜色不再改变,说明NO2的浓度不变,即反应达到平衡状态,不符合题意,B错误;
C.反应前后气体的化学计量数之和不相等,随着反应的进行,容器中的压强不断变化,当容器中的压强不再改变时,说明反应已达到平衡状态,不符合题意,C错误;
D.反应前后气体的化学计量数之和不相等,气体的质量始终不变,随着反应的进行,气体的物质的量不断变化,当气体的物质的量不再改变时,混合气体的平均摩尔质量不再变,说明反应已达到平衡状态,不符合题意,D错误;
答案选A。


科目:高中化学 来源: 题型:
【题目】铁及铁的化合物在生活、生产中具有广泛应用,如亚铁氰化钾即K4[Fe(CN)6]是食盐中常用的抗结剂、铁基(氟掺杂镨氧铁砷化合物)是高温超导材料、“愚人金”是制备硫酸的主要矿物原料。请按要求回答下列问题。
(1)K4[Fe(CN)6]配合物中存在的作用力类型有__________________________(从“金属键”、“离子键”、“共价键”、“配位键”、“氢键”、“范德华力”中选填);其中CN-中各原子最外层均满足8电子稳定结构,其电子式为_____________,其中C原子的杂化形式是_________。
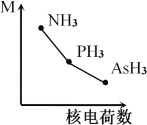
(2)铁基化合物中氟、氧、砷三种元素中电负性值由大到小的顺序是_____________(填元素符号)。其中氢化物(RH3)的某种性能(M)随R的核电荷数的变化趋势如图所示,则纵轴M可能表示为_____________________(从“沸点”、“稳定性”、“分子间作用力”、“R—H键能”中选填)。
(3)FeCl3晶体熔点为306℃,而FeF3晶体熔点高于1000℃,试解释两种化合物熔点差异较大的原因:____________________________________________。
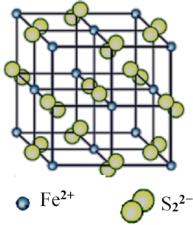
(4)“愚人金”是铁硫化合物,其晶体的晶胞如图所示。该晶体的化学式______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一定温度下的定容容器中,反应:A(s)+2B(g)![]() C(g) +D(g)。下列不能表明反应
C(g) +D(g)。下列不能表明反应
达到平衡状态的是( )。
A.气体的压强不变B.气体平均相对分子质量不变
C.气体的密度不变D.B物质的量浓度不变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关化学用语正确的是 ( )
A. NaOH的电子式:![]()
B. I4O9(碘酸碘)中碘的化合价为+1、+5
C. NH5的结构与NH4Cl相似,NH5的结构式为
D. 离子结构示意图![]() 可以表示35Cl-,也可以表示37Cl-
可以表示35Cl-,也可以表示37Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是可逆反应![]() 在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
在反应过程中的反应速率(v)与时间(t)的关系曲线,下列叙述正确的是( )
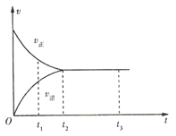
A.t1时,反应只向正方向进行B.t2时,反应未达到限度
C.t2~t3,反应已停止D.t2~t3,各物质的浓度不再发生变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】25C时,0.1mol/L的3种溶液①盐酸②氨水③CH3COONa溶液。下列说法中,不正确的是
A. 3种溶液中pH最小的是①
B. 3种溶液中水的电离程度最大的是③
C. ①与②等体积混合后溶液显酸性
D. ①与③等体积混合后c(Na+)>c(Cl-)>c(H+)>c(CH3COO-)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知HA的酸性比HB弱,在物质的量浓度均为0.1mol·L-1的NaA和NaB混合溶液中,下列排序正确的是( )
A.c(OH-)>c(HA)>c(HB)>c(H+)
B.c(OH-)>c(A-)>c(B-)>c(H+)
C.c(OH-)>c(B-)>c(A-)>c(H+)
D.c(OH-)>c(HB)>c(HA)>c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用下列所示装置不能达到有关实验目的的是( )
A.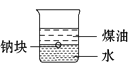 用该装置证明密度ρ(煤油)<ρ(钠)<ρ(水)
用该装置证明密度ρ(煤油)<ρ(钠)<ρ(水)
B. 用该装置可检验HCO3-与CO32-结合H+的难易
用该装置可检验HCO3-与CO32-结合H+的难易
C.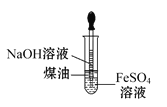 用该装置制备Fe(OH)2
用该装置制备Fe(OH)2
D.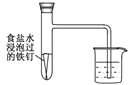 该装置探究钢铁的吸氧腐蚀
该装置探究钢铁的吸氧腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化学平衡原理在工农业生产中发挥着重要的指导作用。
(1)反应C(s)+CO2(g)![]() 2CO(g)平衡常数K的表达式为_______________;
2CO(g)平衡常数K的表达式为_______________;
已知C(s) + H2O(g)![]() CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)
CO(g)+H2(g)的平衡常数为K1;H2(g)+CO2(g)![]() CO(g)+H2O(g)的平衡常数为K2 ,则K与K1、K2二者的关系为_____________________。
CO(g)+H2O(g)的平衡常数为K2 ,则K与K1、K2二者的关系为_____________________。
(2) 已知某温度下,反应2SO2+O2![]() 2SO3,的平衡常数K=19
2SO3,的平衡常数K=19
在该温度下的体积固定的密闭容器中充入c(SO2)=1mol·L-1,c(O2)= 1 mol·L-1,当反应在该温度下SO2转化率为80%时,该反应__________(填“是”或“否”)达到化学平衡状态,若未达到,向__________(填“正反应”或“逆反应”) 方向进行。
(3)对于可逆反应:aA(g) +bB(g)![]() cC(g)+dD(g) △H =akJ·mol-1;
cC(g)+dD(g) △H =akJ·mol-1;
若a+b>c+d,增大压强平衡向_______(填“正反应”或“逆反应”)方向移动;若升高温度,平衡向逆反应方向移动,则a_______0(填“>”或“<”)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com