
A.2HI(g) H2(g)+I2(g);DH>0,若降低温度,颜色加深,压强增大 H2(g)+I2(g);DH>0,若降低温度,颜色加深,压强增大 |
B.2NO2(g) N2O4(g);DH<0,充入氩气,压强增大,红棕色变浅 N2O4(g);DH<0,充入氩气,压强增大,红棕色变浅 |
C.2SO2(g)+O2(g) 2SO3(g);DH<0,升温后,平均相对分子质量减小 2SO3(g);DH<0,升温后,平均相对分子质量减小 |
D.3Fe(s)+4H2O(g) Fe3O4(s)+4H2(g);DH<0,加入铁后,Fe3O4将增加 Fe3O4(s)+4H2(g);DH<0,加入铁后,Fe3O4将增加 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:不详 题型:单选题
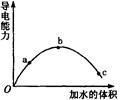
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| t℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
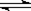 4 C(g) 2min时反应达到平衡状态(温度不变),并测得C 的浓度为0.4 mol/L,请填写下列空白:
4 C(g) 2min时反应达到平衡状态(温度不变),并测得C 的浓度为0.4 mol/L,请填写下列空白:查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 PH3(g) + HI(g) ① ;
PH3(g) + HI(g) ① ;  P4(g)+ 6 H2(g) ② ;
P4(g)+ 6 H2(g) ② ; H2(g) + I2(g) ③
H2(g) + I2(g) ③查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
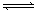 2Z(g);△H<0(正反应为放热反应)。在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是
2Z(g);△H<0(正反应为放热反应)。在不同温度(T1和T2)及压强(P1和P2)下,产物Z的物质的量[n(Z)]与反应时间(t)的关系如图所示。则下列判断正确的是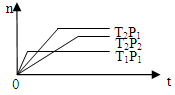
| A.T1<T2,P1<P2 | B.T1<T2,P1>P2 | C.T1>T2,P1>P2 | D.T1>T2,P1<P2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
 2Z(g) △H=-a kJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和1mo1Y2,在500℃对充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。
2Z(g) △H=-a kJ·mol-1(a>0),在一个容积固定的容器中加入2molX2和1mo1Y2,在500℃对充分反应达平衡后Z的浓度为W mol·L-1,放出热量b kJ。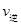 (X2)=2
(X2)=2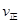 (Y2) d.容器内的密度保持不变
(Y2) d.容器内的密度保持不变查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
 2Z(g)(正反应为放热反应),为了使平衡向生成Z的方向移动,应选择下列的适宜条件是( )
2Z(g)(正反应为放热反应),为了使平衡向生成Z的方向移动,应选择下列的适宜条件是( )| A.①④⑥ | B.②③⑤ | C.①③⑥ | D.②③⑥ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题

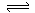 2C0(g) △H>O,K1 ①
2C0(g) △H>O,K1 ①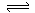 H2(g)+C02(g),K2 ②
H2(g)+C02(g),K2 ②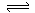 CO(g)+H2(g),K3 ③
CO(g)+H2(g),K3 ③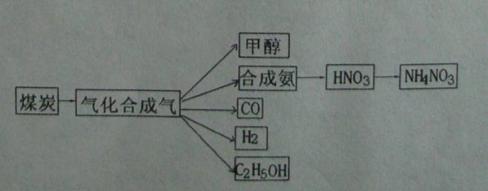

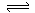 2N02(g) △H>O,在温度为T1、T2时,平衡体系中N02的体积分数随压强变化曲线如图所示。下列说法正确的是( )
2N02(g) △H>O,在温度为T1、T2时,平衡体系中N02的体积分数随压强变化曲线如图所示。下列说法正确的是( )
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com