
A.离子交换法 B.长时间加热
C.加入Na2SO4 D.加入AgNO3
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:
Ⅱ实验室制备氨气,下列方法适宜选用的是________________________。
①固态氯化铵加热分解 ②固体氢氧化钠中滴加浓氨水 ③氯化铵溶液与氢氧化钠溶液共热 ④固态氯化铵与氢氧化钙混合加热
Ⅲ.为了在实验室利用工业原料制备少量氨气,有人设计了如下装置(下图中夹持装置均已略去)。

实验操作:
①检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗中注入一定量稀硫酸。打开弹簧夹c、d、e,则A中有氢气产生。在F出口处收集氢气并检验其纯度。
②关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,放入水槽中,如图6-14所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③用酒精灯加热反应管E,继续通入氢气,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
回答下列问题:
(1)检验氢气纯度的目的是________________________。
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象是___________________。
防止实验装置中压强过大。此时再打开弹簧夹b的原因是_________________,C瓶内气体的成分是_______________。
(3)在步骤③中,先加热铁触媒的原因是__________________。反应管E中发生反应,化学方程式是______________________。
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
Ⅱ.实验室制备氨气,下列方法适宜选用的是_____________________。
①固态氯化铵加热分解 ②固体氢氧化钠中滴加浓氨水 ③氯化铵溶液与氢氧化钠溶液共热 ④固态氯化铵与氢氧化钙混合加热
Ⅲ.为了在实验室利用工业原料制备少量氨气,有人设计了如图6-25装置(图中夹持装置均已略去)。

图6-25
实验操作:
①检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗中注入一定量稀硫酸。打开弹簧夹c、d、e,则A中有氢气产生。在F出口处收集氢气并检验其纯度。
②关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,放入水槽中,如图6-25所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③用酒精灯加热反应管E,继续通入氢气,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
回答下列问题:
(1)检验氢气纯度的目的是____________________________________________。
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象是______________________,防止实验装置中压强过大。此时再打开弹簧夹b的原因是__________________________,C瓶内气体的成分是_______________________。
(3)在步骤③中,先加热铁触媒的原因是_________________。反应管E中发生反应,化学方程式是____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
Ⅱ.实验室制备氨气,下列方法适宜选用的是______________。?
①加热分解固态氯化铵 ②向固体氢氧化钠中滴加浓氨水 ③氯化铵溶液与氢氧化钠溶液共热?④固态氯化铵与氢氧化钙混合加热?
Ⅲ.为了在实验室利用工业原料制备少量氨气,有人设计了如下装置(图中夹持装置均已略去)。?

[实验操作]?
①检查实验装置的气密性后,关闭弹簧夹a、b、c、d、e。在A中加入锌粒,向长颈漏斗中注入一定量稀硫酸。打开弹簧夹c、d、e,则A中有氢气产生。在F出口处收集氢气并检验其纯度。?
②关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③用酒精灯加热反应管E,继续通氢气,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。?
完成下列问题:?
(1)检验氢气纯度的目的是______________。?
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象是______________,防止了实验装置中压强过大。此时再打开弹簧夹b的原因是________________________________________,C瓶内气体的成分是______________。?
(3)在步骤③中,先加热铁触媒的原因是____________________________。反应管E中发生反应的化学方程式是____________________________。
查看答案和解析>>
科目:高中化学 来源:2014届天津市高三上学期第一次月考化学试卷(解析版) 题型:实验题
实验题:I、下列方法适用于实验室中制备氨气的是____________________
A.固态氯化铵加热分解 B.向固体氢氧化钠中滴加浓氨水
C.氯化铵溶液与氢氧化钠溶液共热 D.固体氯化铵与氢氧化钙固体混合加热
II、为了在实验室中利用工业原料制备少量氨气,有人设计了如图所示的装置(图中夹持装置均已略去)。
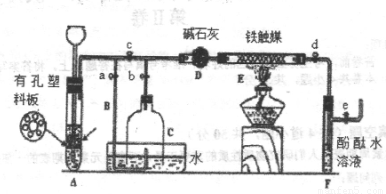
实验操作如下:
①检查装置的气密性后,关闭弹簧夹A.B.C.D.e。在A中加入锌粒,向长颈漏斗注入一定量的稀硫酸。打开弹簧夹C.D.e,则A中有氢气产生。在F出口处收集到氢气并检验其纯度。
②关闭弹簧夹c,取下截去底部的细口瓶C,打开弹簧夹a,将氢气经导管B验纯后点燃,然后立即罩上无底细口瓶C,塞紧瓶塞,如图所示。氢气继续在瓶内燃烧,几分钟后火焰熄灭。
③用酒精灯加热反应管E,继续通入氢气,待无底细口瓶C内水位下降到液面保持不变时,打开弹簧夹b,无底细口瓶C内气体经D进入反应管E,片刻后F中的溶液变红。
请回答下列问题:
(1)写出反应管E中发生反应的化学方程式_______________________________________
用方程式解释F中溶液变红的原因______________________________________________
(2)C瓶内水位下降到液面保持不变时,A装置内发生的现象为____________________________,防止了实验装置中压强过大。此时再打开弹簧夹b的原因是_____________________________________,,C中气体的主要成分为.__________________________________________.
(3)为什么用酒精灯加热反应管E-段时间后再打开弹簧夹b____________________________
(4)为什么F装置不用防倒吸的装置_________________________________________________
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com