
由于具有超低耗电量、寿命长的特点,LED产品越来越受人欢迎,下图是氢氧燃料电池驱动LED发光的装置。下列有关叙述正确的是( )
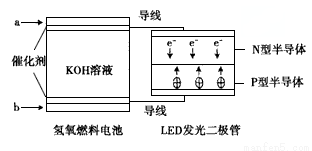
A.电池负极电极反应式为H2-2e-+2OH-=2H2O
B.a处通入氧气,b处通入氢气
C.该装置中能量转化只涉及两种形式的能量
D.P一型半导体连接的是电池负极
 开心口算题卡系列答案
开心口算题卡系列答案 口算题卡河北少年儿童出版社系列答案
口算题卡河北少年儿童出版社系列答案 A加金题 系列答案
A加金题 系列答案科目:高中化学 来源:2016-2017学年吉林长春外国语学校高一上期末理化学卷(解析版) 题型:选择题
有两个无标签的试剂瓶,分别装有Na2CO3和NaHCO3固体,有四位同学为鉴别它们采用以下不同方 法,其中不可行的是( )
法,其中不可行的是( )
A.分别将它们 配制成溶液,再加入澄清石灰水
B.分别将它们配制成溶液,再逐滴加入等浓度的稀盐酸
C.分别将它们配制成溶液,再加入CaCl2溶液
D.分别加热,再用石灰水检验是否有CO2产生
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高一上学期期末化学试卷(解析版) 题型:实验题
某同学帮助水质检测站配制480 mL 0.5 mol·L-1NaOH溶液以备使用。
(1)该同学应选择________mL的容量瓶。使用容量瓶前必须进行的一步操作是______________
(2)其操作步骤如下图所示,则如图操作应在下图中的____________(填选项字母)之间。
A.②与③ B.①与② C.④与⑤
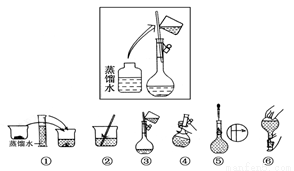
(3)该同学应称取NaOH固体________g
(4)下列操作对所配溶液的浓度大小有何影响?用“偏高”“偏低”或“无影响”填空:
①定容时俯视刻度线:_____________;
②摇匀后,液面低于刻度线,没有再加水:______________;
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高一上学期期末化学试卷(解析版) 题型:选择题
下列说法一定正确的是()
A.0.5mol Cl2所占体积约为11.2 L
B.16g O2中含有的分子数约为6.02×1023
O2中含有的分子数约为6.02×1023
C.0.1mol/L NaCl溶液中含溶质的物质的量为0.1mol
D.标准状况下,11.2 L N2和CO的混合气体所含原子数约 为6.02×1023
为6.02×1023
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上学期期末化学试卷(解析版) 题型:填空题
化学电池在通讯、交通及日常生活中有着广泛的应用。
(1)下列相关说法正确的是 (填序号)。
A.通过某种电池单位质量或单位体积所能输出能量的多少,可以判断该电池的优劣
B.二次电池又称充电电池或蓄电池,这类电池可无限次重复使用
C.除氢气外,甲醇、汽油、氧气等都可用作燃料电池的燃料
D.近年来,废电池必须进行集中处理的问题被提到议事日程,其首要原因是电池外壳的金属材料需要回收
(2)目前常用的镍(Ni)镉(Cd)电池,其电池总反应可表示为:
2Ni(OH)2 +Cd(OH)2 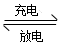 Cd+2NiO(OH)+2H2O
Cd+2NiO(OH)+2H2O
已知Ni(OH)2 和Cd(OH)2 均难溶于水,但能溶于酸,以下说法正确的是___________。
A.电池放电时Cd作负极 B.反应环境为碱性
C. 以上反应是可逆反应 D.该电池是一种二次电池
(3)在宇宙飞船和其他航天器上经常使用的氢氧燃料电池是一种新型电源,其构造如图所示:a、b两个电极均由多孔的碳块组成,通入的氢气和氧气由孔隙中逸入,并在电极表面发生反应而放电。
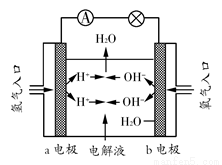
①a电极是电源的________极;
②若该电池为飞行员提供了360kg的水,则电路中通过了________mol电子。
③已知H2的燃烧热为285.8kJ·mol-1,则该燃料电池工作产生36gH2O时,实际上产生了468.8kJ的电能,则该燃料电池的能量转化率是 。(准确到0.01)(能量转化率是实际上释放的电能和理论上反应放出的热能的比率)
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上学期期末化学试卷(解析版) 题型:选择题
某密闭容器中充入等物质的量的气体A和B,一定温度下发生反应A(g)+xB(g)  2C(g),达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化的关系如图所示。下列说法正确的是( )
2C(g),达到平衡后,只改变反应的一个条件,测得容器中各物质的浓度、反应速率随时间变化的关系如图所示。下列说法正确的是( )
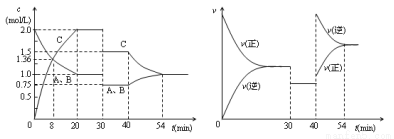
A.前20min B的平均反应速率为0.05mol·L-1·min-1
B.8 min时表示正反应速率等于逆反应速率
C.反应方程式中的x=1,30 min时表示增大压强
D.40 min时改变的条件是升高温度,且正反应为吸热反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年吉林省高二上学期期末化学试卷(解析版) 题型:选择题
下列反应一定不能自发的是( )
A.2KClO3(s)═2KCl(s)+3O2(g)
△H=-78.03kJ·mol-1 △S=+1110 J·mol-1·K-1
B.CO(g)═C(s,石墨)+  O2(g)
O2(g)
△H=+110.5kJ·mol-1 △S=-89.36 J·mol-1·K-1
C.4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)
△H=-444.3kJ·mol-1 △S=-280.1 J.mol-1·K-1
D.NH4HCO3(s)+CH3COOH(aq)═CO2(g)+CH3COONH4(aq)+H2O(l)
△H=+37.301kJ·mol-1 △S=+184.05 J·mol-1·K-1
查看答案和解析>>
科目:高中化学 来源:2016-2017学年四川省乐山市高一上学期教学质检化学试卷(解析版) 题型:选择题
下列条件下,两物质所含分子数不相等的是 ( )
A.同温度、相同质量的N2和CO
B.常温常压,同体积的H2O和O2
C.同压强、同物质的量的N2和O2
D.同温度、同压强、同体积的N2O和CO2
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山西省等三校高二上第二次联考化学试卷(解析版) 题型:选择题
将固体NH4I置于密闭容器中,在一定温度下发生下列反应:
①NH4I(s) NH3(g)+HI(g);
NH3(g)+HI(g);
②2HI(g) H2 (g)+I2(g);
H2 (g)+I2(g);
③2NH3(g) N2(g)+3H2 (g)。
N2(g)+3H2 (g)。
达到平衡时,c(H2) = 2 mol/L,c(N2)=0.5mol/L ,c(HI)=4mol/L,则平衡时 NH3的浓度为
A 0.5 mol • L-1 B.2 mol • L-1 C.4 mol • L-1 D.5 mol • L-1
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com