
【题目】在无色透明的强酸性溶液中,能大量共存的离子组是
A. NH4+、Mg2+、SO42-、NO3- B. Ba2+、Na+、OH-、Cl-
C. K+、NH4+、MnO4-、SO42- D. K +、Na+、NO3-、HCO3-
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】Ⅰ.碘化亚铜(Cu2I2)是一种不溶于水也不溶于酸的白色固体,用途很广泛。完成下列填空:
(1)碘化钾溶液中滴加适量硫酸铜溶液,就能得到碘化亚铜。写出该反应的化学方程式: _________。
(2)往上述反应后溶液中加入淀粉,溶液变蓝,再滴加亚硫酸溶液,蓝色又褪去。写出KI、Cu2I2、H2SO3的还原性由强到弱的顺序是______________。
(3)碘化亚铜能用于检测空气中的汞蒸气,其反应为2Cu2I2+Hg===Cu2HgI4(玫瑰红)+ 2Cu,产物Cu2HgI4中Cu元素显_______价,当有1 mol Cu2I2参与反应时,转移电子数目______。
Ⅱ、过氧化钙可以用于改善地表水质,为测定过氧化钙产品中CaO2的含量,进行如下的实验步骤:
第一步:准确称取a g产品于有塞锥形瓶中,加入适量蒸馏水和过量的b g KI晶体,再滴入少量2 mol·L-1的H2SO4溶液,充分反应。
第二步:向上述锥形瓶中加入几滴淀粉溶液。
第三步:逐滴加入浓度为c mol·L-1的Na2S2O3溶液至反应完全,消耗Na2S2O3溶液V mL。
(已知:I2+2S2O32-=2I-+S4O62-)
(4)第一步发生反应的化学方程式为______________________________;
(5)样品中CaO2的质量分数为____________(用字母表示)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢气是一种清洁能源.制氢和储氢作为氢能利用的关键技术,是当前科学家主要关注的热点问题.
(1)用甲烷制取氢气的两步反应的能量变化如图所示: 
①甲烷和水蒸气反应生成二氧化碳和氢气的热化学方程式是 .
②第Ⅱ步反应为可逆反应.800℃时,若CO的起始浓度为2.0molL﹣1 , 水蒸气的起始浓度为3.0molL﹣1 , 达到化学平衡状态后,测得CO2的浓度为1.2molL﹣1 , 则CO的平衡转化率为 .
(2)NaBH4是一种重要的储氢载体,能与水反应生成NaBO2 , 且反应前后B元素的化合价不变,该反应的化学方程式为 , 反应消耗1mol NaBH4时转移的电子数目为 .
(3)储氢还可借助有机物,如利用环已烷和苯之间的可逆反应来实现脱氢和加氢. 
在某温度下,向恒容容器中加入环已烷,其起始浓度为a molL﹣1 , 平衡时苯的浓度为b molL﹣1 , 该反应的平衡常数K=(用含a、b的关系式表达).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%.目前,消除大气污染有多种方法.
(1)处理NOx的一种方法是利用甲烷催化还原NOx . 已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g)△H=﹣574kJmol﹣1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g)△H=﹣1160kJmol﹣1
则甲烷直接将NO2还原为N2的热化学方程式为 .
(2)利用反应6NO2+8NH3 ![]() 7N2+12H2O处理NO2 . 当转移1.2mol电子时,消耗的NO2在标准状况下是 L.NO2也可用NaOH溶液吸收,生成两种盐,该反应的化学方程式为: .
7N2+12H2O处理NO2 . 当转移1.2mol电子时,消耗的NO2在标准状况下是 L.NO2也可用NaOH溶液吸收,生成两种盐,该反应的化学方程式为: .
(3)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:2NO(g)+2CO(g)N2(g)+2CO2(g);△H<0.该反应的化学平衡常数表达式为K= , 该反应△S0(填“>”或“<”)若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如图所示.若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将移动(填“向左”、“向右”或“不”).20min时,若改变反应条件,导致N2浓度发生如图所示的变化,则改变的条件可能是(填序号).
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的量
(4)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42﹣而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4).已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2++O2+4H+=4Fe3++2H2O,则另一反应的离子方程式为 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期主族元素X、Y、Z、W在元素周期表中的相对位置如图所示。已知X的最低负价与Y的最髙正价代数和为零,下列说法正确的是
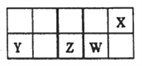
A. X分别与Z、W形成的化合物熔点顺序:Z>W
B. 原子半径的大小顺序:r(X)>r(Y)>r(Z)>r(W)
C. Z的最高价氧化物的水化物酸性比W的强
D. X的简单气态氢化物的稳定性比W的弱
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有关胶体的认识不正确的是( )
A. FeCl3饱和溶液滴入沸水可制得胶体 B. 胶体粒子直径在1~100 nm之间
C. 胶体粒子可以透过滤纸 D. 是否有丁达尔现象是胶体和溶液的本质区别
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】燃料电池型呼气酒精测试仪具有稳定性好,精度高,抗干扰性好等优点,是专门为警察设计的一款执法的检测工具,如图所示是一种酸性燃料电池酒精检测仪的示意图。下列说法错误的是( )
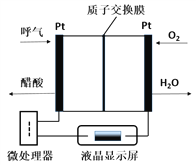
A. 该电池的负极反应式为:CH3CH2OH-4e-+H2O=CH3COOH+4H+
B. 当电路中有0.4mol电子转移时,消耗3.2gO2
C. 电池工作时H+从右向左通过质子交换膜
D. 微处理器通过检测电流大小可计算出被测气体中酒精的含量
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com