
【题目】针对网络上流传的隔夜熟肉中因亚硝酸钠(NaNO2)含量严重超标而不能食用的说法,某兴趣小组开展如下探究活动: 活动一:查阅资料:NaNO2有毒,溶液显碱性,NaNO2有较强的氧化性和较弱的还原性.国家规定肉制品中NaNO2含量不能超过30mg/kg.
(1)NaNO2溶液显碱性的原因是 . (用离子方程式表达) 活动二:鉴别NaNO2与食盐
(2)可用稀硫酸、淀粉和KI溶液鉴别,溶液变蓝的是 . (填化学式).
(3)活动三:检测熟肉中NaNO2含量的变化 分别从 1000g刚煮熟的肉和 1000g隔夜熟肉中提取NaNO2 , 配成溶液,再分别用0.00500mol/L酸性高锰酸钾溶液滴定,刚煮熟的肉消耗12.00mL,隔夜熟肉消耗16.00mL.(提示:MnO4-转化为Mn2+ , NO2-转化为NO3-)
①在做该滴定实验时需要用到的实验仪器有
A.容量瓶 B.酸式滴定管 C.碱式滴定管D.分液漏斗 E.锥形瓶 F. 烧瓶
②滴定终点的判断依据为 .
③隔夜熟肉中NaNO2的含量是mg/kg (保留三位有效数字),该数据说明保存得当的隔夜熟肉(选填“能”或“不能”)食用.
【答案】
(1)NO2﹣+H2O?HNO2+OH﹣
(2)NaNO2
(3)BE;(滴入最后一滴标准液时)锥形瓶内溶液变红,且30秒内不褪色;13.8;能
【解析】解:(1)NaNO2为强碱弱酸盐,亚硝酸根离子能发生水解,水解的离子方程式为NO2﹣+H2OHNO2+OH﹣,
所以答案是:NO2﹣+H2OHNO2+OH﹣;(2)NaNO2有氧化性,能将碘离子氧化成碘单质,所以要酸性条件下,NaNO2能使淀粉、KI溶液变蓝,
所以答案是:NaNO2;(3)①根据氧化还原滴定的操作可知,用到的仪器为酸式滴定管、锥形瓶;
所以答案是:BE;
②因为高锰酸钾的稀溶液是红色的,所以滴定终点时,溶液会出现红色,所以滴定终点的判断依据为:(滴入最后一滴标准液时)锥形瓶内溶液变红,且30秒内不褪色,
所以答案是:(滴入最后一滴标准液时)锥形瓶内溶液变红,且30秒内不褪色;
③根据题意可知,与隔夜熟肉中提取的NaNO2反应的KMnO4的物质的量为0.00500mol/L×0.016L=8.0×10﹣5 mol,根据电子得失守恒可知关系式2KMnO4~5NaNO2,由关系式可知亚硝酸钠的质量为 ![]() ×8.0×10﹣5 mol×69g/mol=13.8mg,所以隔夜熟肉中NaNO2的含量为
×8.0×10﹣5 mol×69g/mol=13.8mg,所以隔夜熟肉中NaNO2的含量为 ![]() =13.8mg/Kg<30mg/kg,所以能食用,
=13.8mg/Kg<30mg/kg,所以能食用,
所以答案是:13.8;能.


科目:高中化学 来源: 题型:
【题目】室温时,CaCO3在水中的溶解平衡曲线如图所示,已知:25℃其溶度积为2.8×10﹣9 mol2/L2 , 下列说法不正确的是( ) 
A.x数值为2×10﹣5
B.c点时有碳酸钙沉淀生成
C.加入蒸馏水可使溶液由d点变到a点
D.b点与d点对应的溶度积相等
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】三氟化硼是平面正三角形,因此是非极性分子,推断三氯甲烷(碳原子位于分子结构中心)的结构和分子的极性情况是( )
A. 四面体,极性分子 B. 平面三角形,非极性分子
C. 正四面体,非极性分子 D. 平面三角形,极性分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在C2H2、C6H6、C2H4O组成的混合物中,已知氧元素的质量分数为8%,则混合物中碳元素的质量分数是( )
A.92.3%
B.87.6%
C.75%
D.84%
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】纳米CaCO3作为工业上重要的无机填充材料,广泛应用于橡胶、塑料、涂料、油墨和造纸等行业。某化学兴趣小组在实验室中利用下列装置模拟工业制备纳米CaCO3.
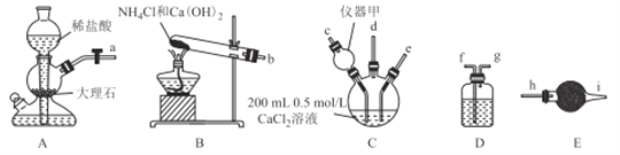
请回答下列问题:
(1)仪器甲的名称是________,在该实验中,其作用是_____.
(2)将上述接口连接顺序补充完整:a![]() ;b
;b![]() ;d
;d![]() 。__________
。__________
(3)装置D中选择的试剂是__________(填序号,下同),装置E中选择的试剂是__________
①饱和Na2CO3溶液 ②饱和NaHCO3溶液 ③无水CaCl2固体 ④碱石灰
(4)装置C中发生反应的离子方程式为__________
(5)随着气体的通入,三颈烧瓶中产生白色沉淀且逐渐增多,但一段时间后,白色沉淀逐渐减少,其可能的原因为_______(结合化学用语解释)。
(6)当生成5g沉淀时,理论上消耗两种气体(标准状况下)的总体积可能为_________
(7)已知:常温下,Ksp(CaCO3)=2.8×10-9,Ksp(CaSO3)=1.4×10-7。向浓度为1.0mol/L的Na2SO3溶液中加入纳米CaCO3,若使CaCO3向CaSO3转化,则该混合液中c(SO32-)/c(CO32-)的值(x)的取值范围为__________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】能用离子方程式Ba2++SO42﹣→BaSO4↓表示的是( )
A.氯化钡和硫酸钠溶液反应
B.碳酸钡和稀硫酸反应
C.氢氧化钡和硫酸铝溶液反应
D.氢氧化钡和稀硫酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验装置正确且能达到实验目的的是( )
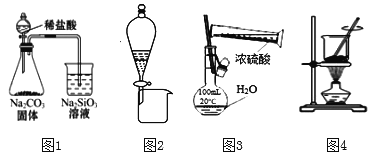
A. 用图1装置证明非金属性Cl>C>Si
B. 利用图2装置,用饱和碳酸钠溶液分离乙醇和乙酸乙酯混合液
C. 图3为配制100 mL一定浓度硫酸溶液
D. 用图4装置灼烧海带
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com