
��14�֣�ʵ���ҿ����ø�����غ�Ũ���ᷴӦ��ȡ��������Ӧ�Ļ�ѧ����ʽ���£�
2KMnO4 +16HCl(Ũ) 2KCl + 2MnCl2 + 5Cl2�� +8H2O
��1���õ����ŷ��������ת�Ƶķ������Ŀ��
��2���÷�Ӧ�е��������뻹ԭ�����ʵ���֮���� ��
��3��KMnO4�������Ա�Cl2�������� ��ѡ�ǿ������������
��4���練Ӧ��ת����2mol���ӣ��������Cl2�ڱ�״�������Ϊ L��
��5��ijͬѧ����KMnO4��������100 mL0.5mol.L-1����Һ���ش��������⣺
������KMnO4��Һʱ���õ���Ҫ������������ƽ��ҩ�ס��ձ�������������Ͳ�� �� ��
��Ӧ��������ƽ��ȡKMnO4���� g��
�۲��淶��ʵ������ᵼ��ʵ���������������в�����ʵ������Ӱ��ƫС���ǣ�������ţ� ��
A����ˮ����ʱ���ӿ̶���
B������ƿ�ڱڸ���ˮ���δ���ﴦ��
C���ߵ�ҡ�Ⱥ��ְ�Һ����ڿ̶����ּ�ˮ����
D�����ܽ������������Һ�彦���ձ���
��1��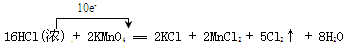 ��2��1:5 ��3��ǿ��4��22.4
��2��1:5 ��3��ǿ��4��22.4
��5���ٽ�ͷ�ι� 100mL����ƿ ��1+1�֣���7.9g ��CD ������ÿ��2�֣���14�֣�
��������
�����������1���õ����ŷ��������ת�Ƶķ������Ŀ��Ҫע����Ӵӻ�ԭ��ָ��������������ֻ�������ӵĸ�����ע����Ӧԭ�ӵĸ�������2���÷�Ӧ��������ǻ�ԭ������������ã��ӻ��ϼ۱仯������ֻ��10����ԭ�ӵĻ��ϼ۸ı��ˣ�����10����HCl����ԭ�������������뻹ԭ�����ʵ���֮����1:5����3������������ԭ��Ӧ����������������Ҫǿ����������������ԣ�����KMnO4�������Ա�Cl2��������Ҫǿ����4�����������������ʵ���Ϊn����
2KMnO4 +16HCl(Ũ) 2KCl + 2MnCl2 + 5Cl2�� +8H2O 10e-
5 10
n 2 n=1mol V(Cl2)=1mol��22.4L/mol=22.4L��5������Һ�����ǻ�Ҫ�õ���ͷ�ιܺ�����ƿ������ƿע��Ҫ�����KMnO4����������m=n��M=c��v��M=0.5 mol.L-1��0.1 L��158g/mol=7.9 g�۸��ӻᵼ����Һ�������С��Ũ�Ⱦͱ���ڶ��ݵ�ʱ��Ҫ��ˮ����������ƿ�ڱڸ���ˮ���Ũ��û��Ӱ�죻�ߵ�ҡ����Һ��������仯�����ڷ��Ӽ���������ɵģ��ټ�ˮ��ʹ����Һ�������Ũ�ȱ�С���ܽ������������Һ�彦���ձ���������������ʧ��Ũ�ȱ�С��ѡCD��
���㣺������ԭ��Ӧ�ĸ���͵��ӵ�ת�Ƽ��㡢һ�����ʵ���Ũ����Һ�����ơ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��22.4L���������������ķ�����ΪNA |
| B���������������������Ļ�ѧ�������ƣ����������������л�ԭ�ԣ����������� |
| C�������������Ħ������Ϊ38g |
| D������������������ɼ��Լ��γɵķǼ��Է��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��Ǩ����У��һ��ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
��NAΪ�����ӵ�������ֵ������˵����ȷ����
A����״���£�22.4LN2�к��е�ԭ����Ϊ2NA
B����״���£�11.2 L CCl4�к��еķ�����Ϊ0.5 NA
C�����ʵ���Ũ��Ϊ1 mol��L-1��K2SO4��Һ�У���2 NA��K+
D��23g Na������H2O��Ӧת�Ƶĵ�����ΪNA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ��Ǩ����У��һ��ѧ������������ѧ�Ծ��������棩 ���ͣ�ѡ����
������Һ��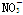 �����ʵ���Ũ��������
�����ʵ���Ũ��������
A��500 mL 1 mol��L��1��KNO3��Һ
B��500 mL 1 mol��L��1��Ba(NO3)2��Һ
C��1000 mL 0.5 mol��L��1��Mg(NO3)2��Һ
D��1 L 0.5 mol��L��1��Fe(NO3)3��Һ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�����и߶���ѧ�����л�ѧ�Ծ��������棩 ���ͣ�ѡ����
����ʵ���ܻ�óɹ�����
 A��������KMnO4��Һ������ϩ����Ȳ
A��������KMnO4��Һ������ϩ����Ȳ
B������м����ˮ����������屽
C���ڱ������������÷�Һ�ķ�������
D����ͭ˿�ھƾ����ϼ��Ⱥ�����������ˮ�Ҵ��У�ͭ˿�ָ���ԭ���ĺ�ɫ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2014-2015����ʡ�߶���ѧ�ڵ�һ��������⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
1 Lij��Һ�к��е��������±���
���� | Cu2�� | Al3�� |
| Cl�� |
���ʵ���Ũ��(mol/L) | 1 | 1 | a | 1 |
�ö��Ե缫������Һ������·����3 mol e��ͨ��ʱ(���Ե��ʱ��Һ����ı仯���缫������ܴ��ڵ��ܽ�����)������˵����ȷ����
A��������Һ������ B��a��3
C����������1.5 mol Cl2 D�����������Ľ�����ͭ����
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com