
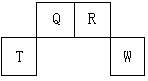
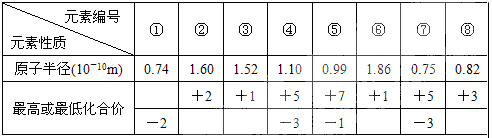



 、
、 。
。 。
。

科目:高中化学 来源:不详 题型:填空题
| ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | ||||||
| 2 | | | | ① | ② | | ③ | | ||||||
| 3 | | ④ | ⑤ | | | ⑥ | ⑦ | ⑧ | ||||||
| 4 | ⑨ | | | | | | ⑩ | |
| 实验步骤 | 实验现象与结论 |
| | |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.16 8O2和18 8O2互为同位素,性质相似 |
| B.将MgCI2溶液蒸干灼烧仍得到MgCI2 |
| C.明矾和漂白粉常用于自来水的处理,两者的作用原理相同 |
| D.C(石墨)=C(金刚石) △H>0,所以石墨比金刚石稳定 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
族 周期 周期 | IA | | 0 | |||||
| 1 | ① | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | |
| 2 | | ② | | ③ | ④ | | ⑤ | |
| 3 | ⑥ | ⑦ | ⑧ | ⑨ | | | ⑩ | |
 比较③、④、⑨的最高价含氧酸的酸性由强到弱的顺序是(用酸的化学式表示) 。
比较③、④、⑨的最高价含氧酸的酸性由强到弱的顺序是(用酸的化学式表示) 。查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题

| A.G是最活泼的非金属单质 | B.L中的化学键是极性键 |
| C.E能使紫色的石蕊试液变蓝 | D.M的化学性质活泼 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.Al14与盐酸反应的化学方程式可表示为:Al14+2HCl= Al14Cl2+H2↑ |
| B.Al13和Al14互为同位素 |
| C.Al13和Al14都具有较强的还原性,容易失去电子生成阳离子 |
| D.Al13超原子中Al原子间通过离子键结合 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com