
��֪A��B��C��DΪ���壬����AΪ����ɫ��D��������ˮ���γɵ���Һ��
ʹ��̪��죬����֮���ת����ϵ����ͼ����ʾ��

��1��������B��ȼ���ѵ�������ʢ������A�ļ���ƿ����Ӧ�����е�ʵ�������� ������ţ�
������ ������ɫ��ȥ ��ƿ���а��� ��ƿ���а���
������ȼ�գ�������ɫ���� ������ȼ�գ�������ɫ����
��2��ʵ������D�Ļ�ѧ����ʽΪ ��
��3��ʵ���ҿ�������ͼ����ʾװ���ռ�D������������ȷ���� ������ţ���
��D���岻������ˮ���ռ�
���������ʢ�м�ʯ��
��ͼ���е�aΪ���ţ��������Ƿ�ֹ�����ݳ�
��4������D�������Ļ�ѧ����ʽΪ ��
��5������E�Ļ�ѧʽ�� ��E���������ʷ��������������������� ������ţ���
�����������������������������������������ǵ����������
��1���٢ڢۢ�
��2��Ca(OH)2 +2NH4Cl 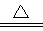 CaCl2+H2O +2NH3��
CaCl2+H2O +2NH3��
��3�� �٢�
��4��4NH3+5O2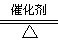 4NO+6H2O
4NO+6H2O
��5��NH4Cl �٢ڢܢ�
��������
���������AΪ����ɫ��D��������ˮ����A��������D�ǰ�����A��B��C��DΪ���壬��B��������C���Ȼ������壬����E���Ȼ�李�
��1�������������а�����ȼ�գ������ɫ������ɫ����ȥ��ƿ���а������Ȼ�������������е�Сˮ�ν�ϣ����֣�ȼ�շ�Ӧ���Ƿ��ȷ�Ӧ������ѡ�٢ڢۢ���
��2��ʵ�����ư����Ļ�ѧ����ʽΪCa(OH)2 +2NH4Cl  CaCl2+H2O +2NH3����
CaCl2+H2O +2NH3����
��3��������������ˮ����������ˮ���ռ�����������ˮ�Լ��ԣ����ü�ʯ�Ҹ��ͼ���е�aӦΪʪ���ɫʯ����ֽ�����鰱���Ƿ��ռ��������Դ�ѡ�٢���
��4�����������������Ļ�ѧ����ʽΪ4NH3+5O2 4NO+6H2O��
4NO+6H2O��
��5��E���Ȼ�泥���ѧʽΪNH4Cl�����ǻ�����Ǵ�������Σ��ǵ���ʣ����Դ�ѡ�٢ڢܢ�
���㣺���������ƶϣ�������������Ӧ������ʵ�����ư��������������ʣ����ʵķ���


 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2016�����ʡפ�����и�һ��ѧ����У������ѧ�Ծ��������棩 ���ͣ�ѡ����
��������ˮ���ռ���������( )
A��H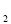 B��O
B��O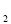 C��NO
C��NO D��NO
D��NO
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�һ��ѧ����ĩ��⻯ѧ�Ծ���A���������棩 ���ͣ�ѡ����
��NA��ʾ�����ӵ�������������������ȷ����
A����״���£�2.24 L CCl4������ԭ����Ϊ0.5 NA
B��100 m L 0.1 mol/L�� NaCl ��Һ�У�����������Ϊ0.02 NA
C��1.7 g ��OH���к��еĵ�����ΪNA
D��78 g Na2O2 ������ˮ��Ӧת�Ƶ�����Ϊ2 NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�һ��ѧ�����п��Ի�ѧ�Ծ���A�����������棩 ���ͣ�ѡ����
��֪������Һ����������Խ��ʱ������Һ���ܶ�Խ��80%��20%������H2SO4��Һ�������Ϻ���Һ����������Ϊ( )
A������50% B������50% C��С��50% D����ȷ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡ�����и�һ��ѧ�����п��Ի�ѧ�Ծ���A�����������棩 ���ͣ�ѡ����
��NA��ʾ�����ӵ�������ֵ������������ȷ����
A������NA����ԭ�ӵĺ����ڱ�״���µ����ԼΪ11.2L
B��25����1.01��105Pa��64gSO2�к��е�ԭ����Ϊ3NA
C���ڳ��³�ѹ�£�11.2LCl2���еķ�����Ϊ0.5NA
D����״���£�11.2LH2O���еķ�����Ϊ0.5NA
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡƽ��ɽ�и�һ��һѧ����ĩ���п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
�������ӷ���ʽ����д��ȷ����
A������ϡ���ᷴӦ��2Fe + 6H+ ��2Fe 3+ +3H 2��
B��NaHCO3��Һ��NaOH��Һ��Ӧ�� OH�D + HCO3- �� CO32- + H2O
C���ƺ���ˮ��Ӧ Na��2H2O��Na+��2OH?��H2��
D���Ȼ�����Һ�м�������İ�ˮAl3+ +4NH3��H2O��AlO2��+4NH4++2H2O
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡƽ��ɽ�и�һ��һѧ����ĩ���п��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
���۵�ʳƷ��װ�г�����һС�����ۣ������������������������������������۵�
A�������� B����ԭ�� C����ˮ�� D��������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�����ʡԭ��У��һ��ѧ����ĩ������ѧ�Ծ��������棩 ���ͣ�ѡ����
������ԭ��Ӧ�У�ˮ�����ÿ���������������ԭ�����������������ǻ�ԭ�����ȷ��������ַǻ�ԭ���ȡ����з�Ӧ��Br2+SO2+2H2O=H2SO4+2HBr��Ƚϣ�ˮ�����ò���ͬ����
A��2Na2O2+2H2O =4NaOH+O2�� B��Cl2 + H2O  HClO + HCl
HClO + HCl
C��2F2+2H2O=4HF+O2 D��4Fe��OH��2+O2+2H2O=4Fe��OH��3
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016��ӱ�ʡ��һ��ѧ�ڵ�һ���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
AZX��A+1ZX+��������������������ȷ����
A��һ�����������ӡ����ӡ�������ɵ�
B����ѧ���ʼ�����ȫ��ͬ
C���˵�����ͺ��������һ�����
D��������һ����ͬ����������������һ������ͬ
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com