
| A. | 食盐和沙子 | B. | 一氧化碳和二氧化碳 | ||
| C. | 铜锌合金 | D. | 氢氧化钠和氢氧化钙 |
分析 混合物的含量测定,可用气体摩尔体积测定完成的是利用混合物中一种成分和加入试剂反应生成气体在标准状况下得到物质的量,依据n=$\frac{m}{M}$计算得到质量,来计算其含量;
解答 解:A、食盐和沙子都是固体,测定成分需要溶解后称量固体质量得到沙子的质量,得到各成分含量,不需要测定气体体积,故A不符合;
B、一氧化碳和二氧化碳都是气体通过氢氧化钠溶液吸收二氧化碳,然后称量增重得到二氧化碳质量,计算成分含量,故B不符合;
C、铜锌合金放入稀硫酸溶液中溶解,利用测定生成的氢气体积测定锌的含量,故C符合;
D、氢氧化钠和氢氧化钙含量测定,利用溶液中复分解反应生成沉淀,称量沉淀质量,计算物质的量得到成分含量,故D不符合;
故选C.
点评 本题考查了气体摩尔体积的应用,主要是成分含量的测定实验过程分析应用,掌握基础是解题关键,题目较简单.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:选择题
| A. | 寒冷的冬天玻璃窗上开出美丽的“窗花” | |
| B. | 石灰浆抹在墙上逐渐变硬 | |
| C. | 樟脑丸在衣柜中长期放置升华 | |
| D. | 闷热的夏天空调出风口飘散出“云雾” |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 阿伏加德罗曾经总结出一条重要定律:同温同压下,同体积的任何气体含有相同数目的分子,右图是电解水的简易装置.
阿伏加德罗曾经总结出一条重要定律:同温同压下,同体积的任何气体含有相同数目的分子,右图是电解水的简易装置.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1:2:3 | B. | 3:2:1 | C. | 1:1:1 | D. | 无法计算 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源:2017届海南省高三上学期月考三化学试卷(解析版) 题型:选择题
某铁的氧化物样品,用5mol/L的盐酸140mL恰好完 全溶解,所得溶液还能吸收0.56L氯气(STP),使其中的Fe2+全部转化为Fe3+。则该氧化物的化学式为( )
全溶解,所得溶液还能吸收0.56L氯气(STP),使其中的Fe2+全部转化为Fe3+。则该氧化物的化学式为( )
A.Fe5O7 B.Fe2O3 C.Fe3O4 D. Fe4O5
查看答案和解析>>
科目:高中化学 来源:2017届广西桂林十八中高三上10月月考化学试卷(解析版) 题型:选择题
下列叙述不正确的是( )
A.钾、钠、镁等活泼金属着火时,不能用泡沫灭火器灭火
B.探究温度对硫代硫酸钠与硫酸反应速率的影响时,若先将两种溶液混合并计时,再用水浴加热至设定温度,则测得的 反应速率偏高
反应速率偏高
C.蒸馏完毕后,应先停止加热,待装置冷却后,停止通水,再拆卸蒸馏装置
D.为准确配制一定物质的量浓度的溶液,定容过程中向容量瓶内加蒸馏水至接近刻度线时,改用滴管滴加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
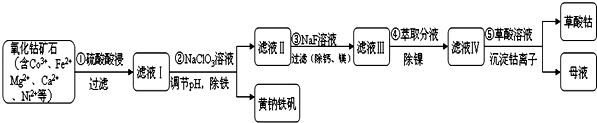
| 序号 | 矿石粒度/目 | 钴浸出率/% |
| 1 | -60 | 9.8 |
| 2 | -120 | 25.5 |
| 3 | -200 | 41.18 |
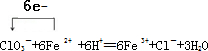 .
.
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com