
| A. | 页岩气是一种新型的能源,主要成分是甲烷和少量液态烃及CO2,使用页岩气可以有效地降低碳排放量,减少温室效应 | |
| B. | 针对H7N9禽流感的扩散情况,要加强环境、个人等的消毒预防,可选用含氯消毒剂、活性银离子、酒精、双氧水等作为消毒剂,这种处理方法符合绿色化学核心 | |
| C. | 李比希基团理论、逆合成分析理论、范特霍夫对有机化合物结构的三维认识都为有机化学的发展作出贡献 | |
| D. | 石油加工工艺除常见的裂化外,还有催化重整和加氢裂化等工艺,它们都是为了提高汽油等轻质油品质;催化重整还是获得芳香烃的主要途径 |
分析 A.甲烷和少量液态烃均可燃烧,二氧化碳的排放可导致温室效应;
B.含氯消毒剂、活性银离子、酒精、双氧水等均可使病毒中蛋白质发生变性,而活性银离子可使人发生重金属中毒;
C.李比希基团理论中官能团决定有机物的性质、是有机物分类的依据;逆合成分析理论使分子转变为一种可能得到的原料的方法;范特霍夫对有机化合物结构的三维认识开创了以有机化合物为研究对象的立体化学;
D.石油裂化得到汽油,催化重整获得芳香烃.
解答 解:A.页岩气是一种新型的能源,主要成分是甲烷和少量液态烃及CO2,二氧化碳的排放可导致温室效应,则使用页岩气可以有效地降低碳排放量,减少温室效应,故A正确;
B.含氯消毒剂、活性银离子、酒精、双氧水等均可使病毒中蛋白质发生变性,而活性银离子可使人发生重金属中毒,则活性银离子处理方法不符合绿色化学核心,故B错误;
C.李比希基团理论中官能团决定有机物的性质、是有机物分类的依据;逆合成分析法从合成产物的分子结构入手,采用“切断一种化学键”分析法,使分子转变为一种可能得到的原料的方法,范特霍夫对有机化合物结构的三维认识开创了以有机化合物为研究对象的立体化学,都为都为有机化学的发展作出贡献,故C正确;
D.石油加工工艺除常见的裂化外,还有催化重整和加氢裂化等工艺,石油裂化得到汽油,催化重整获得芳香烃,故D正确;
故选B.
点评 本题考查物质的性质及应用,为高频考点,把握物质的性质、发生的反应、性质与用途的关系为解答的关键,侧重分析与应用能力的考查,注意化学与生活、环境的联系,选项C为解答的难点,题目难度中等.


科目:高中化学 来源: 题型:选择题
| A. | 该原子的摩尔质量是aNA | |
| B. | Wg该原子的物质的量一定是$\frac{W}{aNA}$mol | |
| C. | 该原子的相对原子质量是$\frac{12}{a}$ | |
| D. | 由已知信息可得:NA=$\frac{12}{a}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol奥沙拉嗪( ) 与足量Na2CO3溶液反应能生成4molC O2B ) 与足量Na2CO3溶液反应能生成4molC O2B | |
| B. | 已知反应mX(g)+nY(g)?qZ(g),若平衡时X、Y的转化率相等,说明反应开始时X、Y的物质的量之比为1:1 | |
| C. | 1L 1mol/LNa2CO3溶液中含有3×6.02×1023个离子 | |
| D. | 在一定温度下,相同pH的硫酸和硫酸铁溶液中水电离出来的c(H+)分别是1.0×10-amol•L-1和是1.0×10-bmol•L-1,在此温度时,水的离子积为1.0×10-(b+a) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 屠呦呦女士通过研究青蒿素获得了“诺贝尔医学奖”以表彰她对疟疾治疗所做的贡献.那么青蒿素的结构式为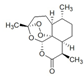 ,分子式为C15H20O5 ,分子式为C15H20O5 | |
| B. | 向鸡蛋清溶液中分别加入(NH4)2SO4和CuSO4溶液都能使鸡蛋清聚沉,其作用原理相同 | |
| C. | 淀粉,纤维素,油脂均能发生水解,同时它们都是高分子化合物 | |
| D. | 在一定条件下,苯与液溴、硝酸、硫酸作用生成溴苯、硝基苯、苯磺酸的反应都属于取代反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1L 0.1mol•L-1的氨水含有0.1 NA个OH- | |
| B. | 常温常压下的33.6L氯气与27g铝充分反应,转移电子数为3NA | |
| C. | 80℃时,1L pH=1的硫酸溶液中,含有0.2NA个H+ | |
| D. | 在电解精炼粗铜的过程中,当阴极析出32g铜时转移电子数为NA |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 稀氯化钙水溶液中 | B. | 氯化银悬浊液中 | ||
| C. | 二氧化硫与氧气反应的混合物中 | D. | 稀醋酸水溶液中 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com