
已知:C(s)+ CO2(g) 2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是 ( )
2CO(g) △H>0。该反应达到平衡后,下列条件有利于反应向正方向进行的是 ( )
| A.升高温度和减小压强 | B.降低温度和减小压强 |
| C.降低温度和增大压强 | D.升高温度和增大压强 |
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:单选题
在反应2A + B 3C +4D中,表示该反应速率最快的是
A.ν(A)=0.5mol/(L·s) B.ν(B)=0.3mol/(L·s)
C.ν(C)=0.8mol/(L·s) D.ν(D)=1mol/(L·s)
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
改变下列条件,能使N2(g)+3H2(g) 2NH3(g) △H<0平衡向逆反应方向移动的是
2NH3(g) △H<0平衡向逆反应方向移动的是
| A.升高温度 | B.增大压强 | C.增大H2的浓度 | D.使用催化剂 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
某可逆反应平衡常数表达式为K=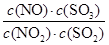 。达到平衡状态时,如果升高温度(其它条件不变),则K值减小。下列说法正确的是( )
。达到平衡状态时,如果升高温度(其它条件不变),则K值减小。下列说法正确的是( )
A.反应的热化学方程式为NO2(g)+SO2(g)  NO(g)+SO3(g) ΔH>0 NO(g)+SO3(g) ΔH>0 |
| B.混合气体的平均摩尔质量保持不变,说明反应已达平衡 |
| C.一定条件下达到平衡时,缩小容器体积,增大体系压强,气体颜色加深 |
| D.使用合适的催化剂可使该反应的反应速率和平衡常数增大 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
在一定温度下,向容积固定不变的密闭容器中充入amolNO2,发生如下反应:
2NO2(g) N2O4(g);△H<0。达平衡后再向容器中充入amolNO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
N2O4(g);△H<0。达平衡后再向容器中充入amolNO2,再次达到平衡后,与原平衡比较,下列叙述不正确的是( )
| A.平均相对分子质量增大 | B.NO2的转化率提高 |
| C.NO2的质量分数增大 | D.反应放出的总热量大于原来的2倍 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
可逆反应2SO2 + O2 2SO3达到一定限度后通入18O2,一段时间18O可能存在于( )
2SO3达到一定限度后通入18O2,一段时间18O可能存在于( )
| A.SO3和O2 中 | B.SO3和SO2 中 |
| C.SO3, SO2和O2 中 | D.SO2和O2 中 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
对于平衡体系mA(g)+nB(g) pC(g)+qD(g) △H<0。下列结论中错误的是( )
pC(g)+qD(g) △H<0。下列结论中错误的是( )
A.若温度不变,将容器的体积缩小到原来的一半,达到新平衡时A的浓度为原来的2.2倍,则m+n<p+q
B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m︰n
C.若m+n=p+q,则向含有a mol气体的平衡体系中再加入a mol的B,达到新平衡时,气体的总物质的量等于2a mol
D.保持其它条件不变,升高温度,平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
T℃时,将6 mol CO2和8 mol H2充入2L密闭容器中,发生反应CO2 ( g ) + 3 H2 ( g )  CH3 OH ( g )+H2O( g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。则下列说法正确的是
CH3 OH ( g )+H2O( g),容器中H2的物质的量随时间变化如图中实线所示。图中虚线表示仅改变某一反应条件时,H2的物质的量随时间的变化。则下列说法正确的是
| A.反应开始至a点时υ(H2) ="1" mol·L-1·min-1 |
| B.曲线II对应的条件改变是降低压强 |
| C.若曲线I对应的条件改变是升温,则该反应△H >0 |
| D.T℃时,该反应的化学平衡常数为0.125 |
查看答案和解析>>
科目:高中化学 来源: 题型:单选题
反应N2O4(g)  2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示。下列说法正确的是 ( )
2NO2(g) ΔH=+57 kJ·mol-1,在温度为T1、T2时,平衡体系中NO2的体积分数随压强的变化曲线如图所示。下列说法正确的是 ( )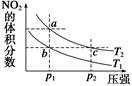
| A.a、c两点的反应速率:a>c |
| B.a、c两点气体的颜色:a深,c浅 |
| C.b、c两点的平衡常数:b<c |
| D.a、c两点气体的平均相对分子质量:a>c |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com