
分析 酯化反应原理为:酸去羟基,醇去氢,若反应物水分子中有同位素${\;}_{\;}^{18}$O,说明酸中含有${\;}_{\;}^{18}$O,据此解答.
解答 解:依据酯化反应原理,酸去羟基,醇去氢,若反应物水分子中有同位素${\;}_{\;}^{18}$O,说明酸中含有${\;}_{\;}^{18}$O,苯甲酸与甲醇反应生成苯甲酸甲酯和水,化学方程式:C6H5-CO18OH+CH3OH$\stackrel{浓硫酸}{→}$C6H5-COOCH3+H218O,
故答案为:C6H5-CO18OH+CH3OH$\stackrel{浓硫酸}{→}$C6H5-COOCH3+H218O.
点评 本题考查了化学方程式书写,明确酯化反应的原理是解题关键,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
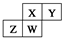 .四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )
.四种元素均为非稀有气体元素.下列关于这四种元素及其化合物的说法中正确的是( )| A. | 原子半径:W>Z>Y>X | |
| B. | 气态氢化物的稳定性:Z>W>X>Y | |
| C. | W的最高正化合价与最低负化合价的绝对值可能相等 | |
| D. | Z的最高价氧化物的水化物可能为强碱 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu$\stackrel{H_{2}SO_{4}}{→}$Cu | B. | Cu$\stackrel{CuSO_{4}}{→}$Ag | C. | Zn$\stackrel{NH_{4}Cl}{→}$C | D. | Zn$\stackrel{C_{2}H_{5}OH}{→}$Cu |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ,1个O22+中含有2个π键.
,1个O22+中含有2个π键.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 原子晶体的熔点一定比金属晶体的高 | |
| B. | 分子晶体的熔点一定比金属晶体的低 | |
| C. | 晶体内部的微粒按一定规律周期性的排列 | |
| D. | 凡有规则外形的固体一定是晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
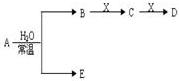 已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去).
已知A、B、C、D、E、X存在如图所示转化关系(部分生成物和反应条件略去). .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
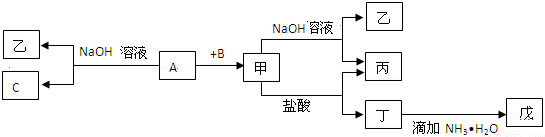
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com