
����Ŀ����������� (Na2S2O3)�����������о��й㷺Ӧ�á���ǹ�ҵ����ȡ��������Ƶķ���֮һ��ʵ����ģ�ҵ����װ����ͼ��ʾ��
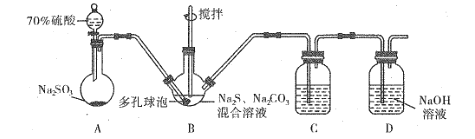
(1)������ͼװ�ý���ʵ�飬Ϊ��֤����˳�����µIJ�����_______��
(2)װ��B�����ɵ�Na2S2O3ͬʱ������CO2����Ӧ�����ӷ���ʽΪ_______���ڸ�װ����ʹ�ö�����ݵ�Ŀ����_____��
(3)װ��C�������Ǽ���װ��B��SO2������Ч����C�п�ѡ����Լ���__(����ĸ)��
a.H2O2��Һ b.��ˮ c.KMnO4��Һ d.BaCl2��Һ
(4)Na2S2O3��Һ�����ڲⶨ��ˮ��Ba2+Ũ�ȡ�
��ȡ��ˮ20.00mL�������ʵ�����ȣ���������K2Cr2O7��Һ���õ� BaCrO4 ����������ϴ�Ӻ�������ϡ���ܽ⣬��ʱ CrO42-ȫ��ת��ΪCr2O72-���ټӹ��� KI��Һ����Cr2O72- ��ַ�Ӧ��Ȼ����������Һ��ָʾ������0.100 mol/L��Na2S2O3 ��Һ���еζ���(I2 +2 S2O32-= S4O62-+ 2I-)���ζ��յ������Ϊ__________��ƽ�еζ�3�Σ�����Na2S2O3 ��Һ��ƽ������Ϊ18.00mL����÷�ˮ��Ba2+ �����ʵ���Ũ��Ϊ____mol/L��
���ڵζ������У�����ʵ����������ʵ����ƫ�ߵ���______(����ĸ)��
a.�ζ���δ��Na2S2O3��Һ��ϴ
b.�ζ��յ�ʱ���Ӷ���
c.��ƿ������ˮϴ�Ӻ�δ���и��ﴦ��
d.�ζ��ܼ��촦�ζ�ǰ�����ݣ��ζ��յ㷢��������
���𰸡���Һ©���ϿڵIJ��������߽������ϰ��۶�©�����ϵ�С�� 4SO2+2S2-+![]() =
=![]() +CO2 ����SO2����Һ�ĽӴ������ʹ��Ӧ��� bc �������һ��Na2S2O3 ��Һ��ɫ��ȥ���ڰ�����ڲ��ָ� 0.03mol/L a
+CO2 ����SO2����Һ�ĽӴ������ʹ��Ӧ��� bc �������һ��Na2S2O3 ��Һ��ɫ��ȥ���ڰ�����ڲ��ָ� 0.03mol/L a
��������
װ��A������Ũ������������Ʒ�Ӧ���ɶ���������Bװ�ã�������ݿ�������������Һ��ĽӴ������װ��B�����ö����������ƺ�̼���Ʒ�Ӧ��ȡ��������ƣ�װ��C����������������Ч������Ҫ�����Ե�ʵ������װ��D����β�����ա�
(4)�ζ������У�![]() �������������ɵⵥ�ʣ�Ȼ�����Na2S2O3��Һ�ζ����ɵĵⵥ�ʵ������Ӷ�ȷ��
�������������ɵⵥ�ʣ�Ȼ�����Na2S2O3��Һ�ζ����ɵĵⵥ�ʵ������Ӷ�ȷ��![]() ����������ȷ�������ӵ�����
����������ȷ�������ӵ�����
(1)��û�д�Һ©���ϿڵIJ���������û�н������ϰ��۶�©�����ϵ�С�ף���Һ©���ڵ�Һ�彫����˳�����£�Ϊ��֤����˳���������Һ©���ϿڵIJ��������߽������ϰ��۶�©�����ϵ�С�ף�
(2)������֪��ϢSO2��Na2S��Na2CO3��Ӧ����Na2S2O3��CO2���ù����ж�����������Ԫ�ػ��ϼ۽��ͣ�������������������Ԫ�ػ��ϼ���������ԭ������ϵ����غ��Ԫ���غ�ɵ����ӷ���ʽΪ��4SO2+2S2-+![]() =
=![]() +CO2���ڸ�װ����ʹ�ö�����ݿ�������Ӵ������ʹ��Ӧ��֣�
+CO2���ڸ�װ����ʹ�ö�����ݿ�������Ӵ������ʹ��Ӧ��֣�
(3)a������������Ա�˫��ˮ��������û����������a��ѡ��
b����ˮ��������������������Һ��ɫ�ᷢ���仯����bѡ��
c��������ؿ�������������������Һ��ɫ�ᷢ���仯����cѡ��
d�������������Ȼ�����Һ����Ӧ����d��ѡ��
��������ѡbc��
(4)�ٵζ��յ�ⵥ�ʱ���ȫ��Ӧ����Һ��ɫ��ȥ�����Եζ��յ������Ϊ���������һ��Na2S2O3 ��Һ��ɫ��ȥ���ڰ�����ڲ��ָ���
![]() �������������ɵⵥ�ʣ���������ԭ��Cr3+��������ת����ϵ
�������������ɵⵥ�ʣ���������ԭ��Cr3+��������ת����ϵ![]() ��3I2���ζ������з�����ӦI2 +
��3I2���ζ������з�����ӦI2 +![]() = S4O62-+ 2I-������I2��
= S4O62-+ 2I-������I2��![]() ����������
����������![]() ����ת����ϵ2Ba2+��2BaCrO4��
����ת����ϵ2Ba2+��2BaCrO4��![]() ������Ba2+��
������Ba2+��![]() ����������ϵ2Ba2+��
����������ϵ2Ba2+��![]() �����Է�Һ��Ba2+��Ũ��Ϊ
�����Է�Һ��Ba2+��Ũ��Ϊ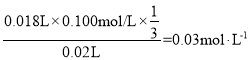 ��
��
��a���ζ���δ�ñ�Һ��ϴ����ϡ�ͱ�Һ���������ı�Һ�����ƫ�ⶨ���ƫ�ߣ�
b���ζ��յ�ʱ���Ӷ������¶���ƫС����ȡ�ı�Һ���ƫС���ⶨ���ƫ�ͣ�
c����ƿ������ˮϴ�Ӻ�δ���и��ﴦ�����Դ���Һ�����ʵ����ʵ���û��Ӱ�죬�ʶ�ʵ������Ӱ�죻
d���ζ��ܼ��촦�ζ�ǰ�����ݣ��ζ��յ㷢�������ݽ�ʹ��ȡ�ı�Һ���ƫС���ⶨ���ƫ�ͣ�
��������ѡa��


 �п�������㾫��ϵ�д�
�п�������㾫��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֦������������о�����ṹ��ʽ��ͼ�����й��ڷ�֦�����������ȷ����
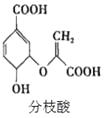
A.�����к���3�ֺ���������
B.��һ�������¿����Ҵ������ᷴӦ,�ҷ�Ӧ������ͬ
C.1mol��֦��������3molNaOH�����кͷ�Ӧ
D.��ʹ������Ȼ�̼��Һ�����Ը��������Һ��ɫ,����ɫԭ����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧ����ʽ����뷽��ʽ�У�������ȷ���ﷴӦ��ɫ�仯����
A.������ͨ����з�̪��Һ��ˮ�У���Һ��죺NH3��H2O![]() NH3��H2O
NH3��H2O![]() NH4����OH��
NH4����OH��
B.����FeCl3��Һ�����ˮ�б�Ϊ���ɫҺ�壺FeCl3��3H2O![]() Fe(OH)3(����)��3HCl
Fe(OH)3(����)��3HCl
C.��CuCl2��Һ�м������������ۣ���Һ����ɫ��Ϊdz��ɫ��Fe��CuCl2��Cu��FeCl2
D.�������ʹ�ú�Na2O2�ɵ���ɫ��Ϊ��ɫ��2Na2O2��2Na2O��O2��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������Ԫ�صĻ��ϼ��Ʋ����ʵ������ǻ�ѧ�о�����Ҫ�ֶ�����ͼ����Ԫ�صij������ϼ��벿���������Ķ�Ӧ��ϵ��
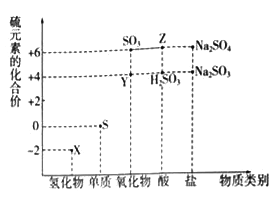
��1������Ԫ�ػ��ϼ۱仯�ĽǶȷ�����ͼ�м������������л�ԭ�ԵĻ�������_______���ѧʽ����
��2����X��Y��ϣ������ɵ���ɫ���壬�÷�Ӧ���������뻹ԭ�������ʵ���֮��Ϊ_______��
��3��Z��Ũ��Һ��ͭ������һ�������¿��Է�����ѧ��Ӧ���÷�Ӧ�Ļ�ѧ����ʽΪ_______��
��4��Na2S2O3����Ҫ�Ļ���ԭ�ϣ���������ԭ��Ӧ�ĽǶȷ����������Ʊ�Na2S2O3�ķ��������Ͽ��е���______������ţ���
a��Na2S+S b��Na2SO3+S c��SO2+Na2SO4 d��Na2SO3+Na2SO4
��5����֪Na2SO3�ܱ�K2Cr2O7����ΪNa2SO4��24mL 0.05molL��1��Na2SO3��Һ�� 20mL 0.02molL��1��K2Cr2O7��Һǡ�÷�Ӧʱ��CrԪ���ڻ�ԭ�����еĻ��ϼ�Ϊ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������������������������Ź㷺��Ӧ�ã�ij��ѧ��ȤС������ͼһװ��̽���������й����ʡ�
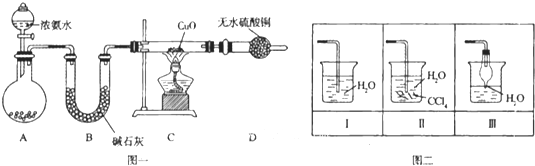
��1��װ��A����ƿ���Լ���ѡ�� �����������B��������
a����ʯ�� b��Ũ���� c����ʯ�� d���ռ���Һ
��2�����Ӻ�װ�ò�����װ�õ������Ժ�װ��ҩƷ��Ȼ��Ӧ�� ����I�������
�����������Բ����ƿ�м��백ˮ ����װ��C
��3��ʵ���й۲쵽C��CuO��ĩ��죬D����ˮ����ͭ���������ռ���һ�ֵ������壬��÷�Ӧ��ػ�ѧ����ʽΪ ,���÷�Ӧ֤���������� �ԣ�
��4����ʵ��ȱ��β������װ�ã�ͼ��������������β����װ���� ����װ���������
��5��������������ˮ������״���£���2.24L�İ�������ˮ���0.5L��Һ��������Һ�����ʵ���Ũ��Ϊ mol/L��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������A(ij����)��ˮ��Һ������������ʾ��һϵ�б仯��

��1��д��A��F���ʵĻ�ѧʽ��
A__________��B__________��C__________��D__________��E.__________��F__________��
��2��д��E��F�Ļ�ѧ����ʽ______________________________��
��3����������F�������ӵķ�����________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ס���������ѧ��ȤС�飬�ֱ����Ҵ�����������֤�����ʵ�顣����ʵ�������ͼ1��ʾ������ʵ�������ͼ2��ʾ���ܱ�ϵͳ�ڿ������١�����д���пհף�


��1������Ҫ���ȫ��ʵ�����ݣ����²�������ȷ��˳���� _____ ������ţ�������ظ�����
�ټ��ȡ��ڼ��װ�õ������ԡ�����A�л����������Ŀ�������ȡ��Dװ��
��2���ס�������ʵ���У�������A~H����Ҫ���ȵ���________�����ţ���
��3����Ӧ��ʼ��C�й۲쵽��������________��
��4��д��E�з�����Ӧ�Ļ�ѧ����ʽ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���������ӵļ��鷽����ȷ����
A.�����Һ���ȼ������ᱵ��Һ�а�ɫ�������ټ���ϡ���ᣬ��ɫ��������ʧ������ȷ�ϴ���Һ�к���SO![]()
B.�����Һ�м���NaOH��Һ�����ȣ�������������ʹʪ��ĺ�ɫʯ����ֽ����������ȷ�ϴ���Һ�к���NH![]()
C.�����Һ���ȼ�����ˮ���ٵ���KSCN��Һ����Һ��죬����ȷ�ϴ���Һ�к���Fe2+
D.�ò�����պȡ����Һ���ھƾ��ƻ��������գ�����ʻ�ɫ������ȷ�ϴ���Һ�к���Na+
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��ѧ��ӦA2(g)��B2(g)=2AB(g)�������仯��ͼ��ʾ���ж�������������ȷ����

A.ÿ����2����AB����bkJ����
B.����1molA-A����1molB-B�����ų�akJ����
C.�÷�Ӧ�з�Ӧ������������ڲ����������
D.�÷�Ӧ��Ϊ(a��b)kJ��mol��1
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com