如图方格中的符号表示一种反应物或生成物(反应时加入或生成的水以及生成沉淀J时的其它产物均已略去).已知F是一种常见金属.
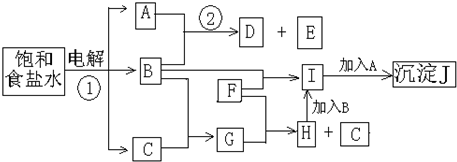
(1)物质A是
NaOH
NaOH
,G是
HCl
HCl
,J是
Fe(OH)3
Fe(OH)3
.
(2)用碳棒作电极电解饱和食盐水时,阳极产物是
氯气
氯气
(写物质名称),检验该电极产物的实验方法是
用湿润的淀粉KI试纸检验,若变蓝,则证明是氯气
用湿润的淀粉KI试纸检验,若变蓝,则证明是氯气
.
(3)反应①的化学方程式
,反应②的化学方程式
Cl2+2NaOH=NaCl+NaClO+H2O
Cl2+2NaOH=NaCl+NaClO+H2O
.



