


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
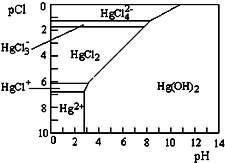 水体中二价汞离子可以与多种阴离子结合成不同的存在形态.水溶液中二价汞主要存在形态与Cl-、OH-的浓度关系如图所示[注:粒子浓度很小时常用负对数表示,如pH=-lgc(H+),pCl=-lgc(Cl-)].
水体中二价汞离子可以与多种阴离子结合成不同的存在形态.水溶液中二价汞主要存在形态与Cl-、OH-的浓度关系如图所示[注:粒子浓度很小时常用负对数表示,如pH=-lgc(H+),pCl=-lgc(Cl-)]. 查看答案和解析>>
科目:高中化学 来源: 题型:
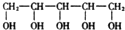 ,下列有关木糖醇的说法正确的是( )
,下列有关木糖醇的说法正确的是( )| A、木糖醇是-种单糖,不能发生水解反应 |
| B、木糖醇易溶解于水,不能发生酯化反应 |
| C、木糖醇在口腔中不易被氧化为酸 |
D、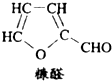 木糖醇脱去三分子水可得糠醛(结构如图) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO2有漂白性 |
| B、SO2溶于水后,溶液呈酸性 |
| C、SO2有还原性 |
| D、SO2有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al3+,Na+,NO3-,Cl- |
| B、K+,Na+,Cl-,NO3- |
| C、K+,Na+,Cl-,CH3COO- |
| D、K+,NH4+,SO42-,NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、三氯化铝溶液中加入过量NaOH溶液:Al3++3OH-═Al(OH)3↓ |
| B、4mol/L的NaAlO2溶液和7mol/L的HCl等体积互相均匀混合:4AlO2-+7H++H2O═3Al(OH)3↓+Al3+ |
| C、K37ClO3与浓盐酸(HCl)在加热时生成氯气:K37ClO3+6HCl=K37Cl+3Cl2↑+3H2O |
| D、将0.1mol/L盐酸数滴缓缓滴入0.1mol/L25mLNa2CO3溶液中,并不断搅拌:2H++CO32-═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、进行中和热测定的实验时,不能用环形铁质搅拌棒代替环形玻璃搅拌棒 |
| B、用等体积的0.50mol?L-1盐酸和0.55mol?L-1NaOH溶液进行中和热测定的实验,会使测定结果偏大 |
| C、已知强酸与强碱反应的中和热△H=-57.3kJ?mol-1.所以,1L 1mol?L-1H2SO4与稀NaOH溶液恰好完全反应时,放出57.3kJ的热量 |
| D、已知2C(s)+O2(g)=2CO(g)△H=-220.7kJ?mol-1;所以,C的燃烧热是△H=-220.7kJ?mol-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com