
【题目】X、Y都是IIA(Be除外)的元素,已知它们的碳酸盐的热分解温度:T(XCO3)>T(YCO3),则下列判断正确的是( )
A. 晶格能: XCO3>YCO3 B. 阳离子半径: X2+>Y2+
C. 金属性: X>Y D. 氧化物的熔点: XO>YO
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
【题目】下列关于氢原子的电子云图的描述中,正确的是 ( )
A. 电子云是一团带负电荷的云雾
B. 每个小黑点表示一个核外电子
C. 小黑点多的区域电子多
D. 小黑点的疏密表示电子在核外单位体积内出现机会的多少
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】金属具有延展性的原因是
A. 金属原子半径都较大,价电子数较少
B. 金属受外力作用变形时,金属阳离子与自由电子间仍保持较强烈的作用
C. 金属中大量自由电子受外力作用时,运动速率加快
D. 自由电子受外力作用时能迅速传递能量
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法不正确的是( )
A. 用浸泡过高锰酸钾溶液的硅藻土保鲜水果,其作用是吸收水果释放出的乙烯
B. 医疗上常用体积分数为75%的酒精溶液作消毒剂
C. 甲醛的水溶液叫做福尔马林,具有杀菌防腐的性能
D. 某些桶装水使用的劣质塑料桶常含有乙二醇,乙二醇不溶于水
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】归纳法是高中化学学习常用的方法之一,某化学研究性学习小组在学习了《化学反应原理》后作出了如下的归纳总结,其中正确的是
①常温下,pH=3的醋酸溶液与pH=11的NaOH溶液等体积混合,则有c (Na+) + c(H+)=c(OH-) + c(CH3COO-)
②对已建立化学平衡的某可逆反应,当改变条件使化学平衡向正反应方向移动时,生成物的百分含量一定增加
③常温下,AgCl在同物质的量浓度的CaCl2和NaCl溶液中的溶解度相同
④常温下,已知醋酸电离平衡常数为Ka;醋酸根水解平衡常数为Kh;水的离子积为Kw;则有:Ka·Kh=Kw
⑤电解精炼铜时,电解质溶液中铜离子浓度不变 。
A.①④ B.①②④ C.①②④⑤ D.①②③④
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】钙和钠相似,也能形成过氧化物,则下列叙述正确的是
A.过氧化钙的化学式是Ca2O2
B.1mol过氧化钠或过氧化钙跟足量水反应都生成0.5mol氧气
C.过氧化钙中钙元素的化合价为+4
D.过氧化钙中属于碱性氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各项表述与示意图形不一致的是

A. 图①表示25℃时,用0.1 mol·L-1盐酸滴定20 mL 0.1 mol·L-1NaOH溶液,溶液pH随加酸体积的变化
B. 图②中曲线表示反应2SO2(g) + O2(g)![]() 2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
2SO3(g);ΔH < 0 正、逆反应的平衡常数K随温度的变化
C. 图③表示10 mL 0.01 mol·L-1KMnO4酸性溶液与过量0.1 mol·L-1草酸溶液混合,n(Mn2+) 随时间的变化
D. 图④中a、b曲线分别表示反应CH2=CH2(g)+ H2(g) →CH3CH3(g);ΔH>0使用和未使用催化剂时,反应过程中的能量变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是NaCl晶体的一个晶胞结构模型,KO2的晶体结构与NaCl的相似,KO2可以看做是Na+的位置被K+代替,Cl-的位置被O2-代替代替。则下列关于K02晶体结构的叙述中正确的是
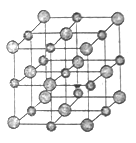
A. 与K+距离相等且最近的O2-有8个
B. 与K+距离相等且最近的O2-构成的多面体是六面体
C. 一个KO2晶胞中的K+和O2-的粒子数都是4个
D. 与K+距离相等且最近的K+有8个
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com