
(6分)根据下表信息回答以下问题:
元素 | A | B | C | D | E | F | G | H |
原子半径(nm) | 0.130 | 0.118 | 0.090 | 0.102 | 0.073 | 0.154 | 0.037 | 0.099 |
主要化合价 | +2 | +3 | +2 | +6,-2 | -2 | +1 | +1 | +7,-1 |
部分短周期元素的原子半径及主要化合价
(1)将A、D、E、F、H对应的简单离子按照半径由小到大的顺序填空________________。
(2)B、H两元素的最高价氧化物所对应的水化物相互反应的离子方程式是____________________。
(3)实验室中制取H单质反应的化学方程式是______________________________。
 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案 学练快车道快乐假期暑假作业新疆人民出版社系列答案
学练快车道快乐假期暑假作业新疆人民出版社系列答案科目:高中化学 来源:2014-2015学年江西省红色六校高三第二次联考理综化学试卷(解析版) 题型:填空题
(15分)(Ⅰ)磷是生物体中不可缺少的元素之一,在自然界中磷总是以磷酸盐的形式出现的,例如磷酸钙矿Ca3(PO4)2、磷灰石Ca5F(PO4)3等。
(1)磷的某种核素中,中子数比质子数多1,则表示该核素的原子符号为____________。
(2)磷酸钙与焦炭、石英砂混合,在电炉中加热到1500℃生成白磷,反应为:
2Ca3(PO4)2+6SiO2 = 6CaSiO3+P4O10 10C+P4O10 = P4↑+10CO↑
上述反应中的各种物质,属于酸性氧化物的有 。
(3)白磷有剧毒,不慎沾到皮肤上,可用CuSO4溶液冲洗解毒。白磷可与热的CuSO4溶液反应生成磷化亚铜,与冷溶液则析出铜,反应方程式分别(均未配平)为:
①P4+CuSO4+H2O→Cu3P+H3PO4+H2SO4
②P4+CuSO4+H2O→Cu+H3PO4+H2SO4
反应①中,氧化剂为 ,若上述两反应中被氧化的P4的物质的量相等,则消耗的CuSO4的物质的量之比为 。
(Ⅱ)离子交换膜是一类具有离子交换功能的高分子材料。一容器被离子交换膜分成左右两部分,如图所示。

若该交换膜为阳离子交换膜(只允许阳离子自由通过),左边充满盐酸酸化的H2O2溶液,右边充满滴有KSCN溶液的FeCl2溶液(足量),一段时间后右边可观察到的现象: ;若该交换膜为阴离子交换膜(只允许阴离子自由通过),左边充满含2mol NH4Al(SO4)2的溶液,右边充满含3mol Ba(OH)2的溶液,当有2mol SO42-通过交换膜时(若反应迅速完全),则左右两室沉淀的物质的量之比为 。
(Ⅲ)某初级石墨中含SiO2(7.8%)、Al2O3(5.1%)、Fe2O3(3.1%)和MgO(0.5%)等杂质,利用相关工艺可进行提纯与综合利用。通入一定量的N2后,在1500℃下与Cl2充分反应得到纯化石墨与气体混合物,然后降温至80℃,分别得到不同状态的两类物质a和b。(注:石墨中氧化物杂质均转变为相应的氯化物,SiCl4的沸点为57.6℃,金属氯化物的沸点均高于150℃。)
(1)若a与过量的NaOH溶液反应,可得两种盐,其中一种盐的水溶液具有粘合性,
化学反应方程式为 _________。
(2)若b与过量的NaOH溶液充分反应后,过滤,所得滤液中阴离子有 _________。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省宿迁市三校高三下学期3月质量检测化学试卷(解析版) 题型:选择题
下列有关化学用语表示正确的是
A.明矾的化学式:KAl(SO4)2
B.氯离子的结构示意图:
C.2 丙醇的结构简式:(CH3)2CHOH
丙醇的结构简式:(CH3)2CHOH
D.溴化铵的电子式:
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省揭阳市高三一模考试理综化学试卷(解析版) 题型:推断题
(16分)用丙酮为原料来合成化合物(B)(其中部分产物未列出)的路线如下:
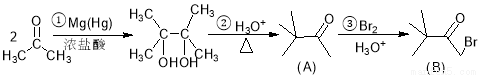
(1)写出反应③的无机产物的化学式 ,化合物(B)所含有官能团的名称 ;
(2)中间产物(A)可经过著名的黄鸣龙还原法,直接得到对应相同碳骨架的烷烃,请写出得到的该烷烃的分子式 ,对该烷烃用系统命名法命名: ;
(3)写出化合物(B)与氢氧化钠的水溶液共热的化学方程式: ;
(4)丙酮同分异构体有多种,其中一种环状的同分异构体发能生加聚反应后得到某种高聚物的结构简式是: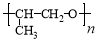 ,则该同分异构体的结构简式为:___________;
,则该同分异构体的结构简式为:___________;
(5)反应②是著名的频哪醇(pinacol)重排,试写出用环戊酮(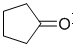 )来代替丙酮,连续发生上述路线中反应①、②之后,得到的有机产物的结构简式为: 。
)来代替丙酮,连续发生上述路线中反应①、②之后,得到的有机产物的结构简式为: 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省揭阳市高三一模考试理综化学试卷(解析版) 题型:选择题
NA表示阿伏加德罗常数的值,下列说法中正确的是
A.1 mol Zn与足量任意浓度的硫酸反应转移电子数均是2 NA
B.在常温常压下1 mol C7H16中含有共价键的总数目是23 NA
C.0.1 mol FeCl3完全水解生成Fe(OH)3胶体粒子数目为0.1NA
D.33.6 L 盐酸在标准状况下所含有HCl分子的数目为1.5 NA
查看答案和解析>>
科目:高中化学 来源:2014-2015河北枣强中学高一上学期期末考试化学试卷(解析版) 题型:选择题
下列两种物质发生反应:①Na和O2 ②AlCl3与氨水 ③水玻璃与CO2 ④Fe与Cl2 ⑤Fe和稀HNO3 ,因反应物用量或反应条件的不同而生成不同产物的是
A.①②③④⑤ B.①②③⑤ C.①②⑤ D.①③⑤
查看答案和解析>>
科目:高中化学 来源:2014-2015河北枣强中学高一上学期期末考试化学试卷(解析版) 题型:选择题
下列有关氨的说法正确的是
A.氨是弱电解质,铵盐是强电解质
B.液氨是纯净物,氨水是混合物
C.氨气遇浓盐酸、浓硫酸、浓硝酸都能产生白烟
D.氨气易液化,所以可用来做喷泉实验
查看答案和解析>>
科目:高中化学 来源:2014-2015河北枣强中学高一上学期期末考试化学试卷(解析版) 题型:选择题
不能与SiO2发生反应的物质是
A.烧碱溶液 B.氧化钙 C.浓硝酸 D.焦炭
查看答案和解析>>
科目:高中化学 来源:2014-2015河北邢台一中高一3月月考化学试卷(解析版) 题型:选择题
根据下列热化学方程式,判断氢化物的稳定性顺序正确的是
N2(g)+3H2 (g)=2NH3(g) ΔH=-92.38 kJ·mol-1
H2(g)+Cl2(g)=2HCl(g) ΔH=-184.72 kJ·mol-1
I2(g)+H2(g)=2HI(g) ΔH=+51.92 kJ·mol-1
A.HI>HCl>NH3 B.HCl>NH3>HI
C.HCl>HI>NH3 D.NH3>HI>HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com