
| A. | H、D、T表示同一种核素 | B. | 次氯酸电子式 | ||
| C. | F原子结构示意图: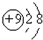 | D. | CH4分子的球棍模型: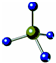 |
分析 A.具有一定质子数和中子数的原子就是一种核素;
B.次氯酸中存在1个氧氢键和1个氧氯键;
C.F的质子数和核外电子数为9;
D.甲烷为正四面体结构,其正确的球棍模型为: .
.
解答 解:A.H、D、T为氢元素的3种不同核素,它们之间互为同位素,故A错误;
B.次氯酸为共价化合物,分子中存在1个氧氢键和氧氯键,次氯酸的电子式为 ,故B错误;
,故B错误;
C.F的原子结构示意图为 ,故C错误;
,故C错误;
D. 为甲烷的比例模型,甲烷的球棍模型应该用小球和短棍表示,甲烷为正四面体结构,其正确的球棍模型为:
为甲烷的比例模型,甲烷的球棍模型应该用小球和短棍表示,甲烷为正四面体结构,其正确的球棍模型为: ,故D正确.
,故D正确.
故选D.
点评 本题考查了核素、电子式、原子结构示意图判断以及球棍模型与比例模型,题目难度中等,注意掌握常见化学用语的表示方法,明确球棍模型与比例模型的区别.


 优加精卷系列答案
优加精卷系列答案科目:高中化学 来源: 题型:解答题
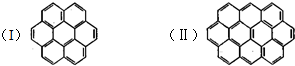 有两个或两个以上的苯环以共有环边的方式相互稠合的多环芳香烃称为稠环芳香烃.下图中椭圆烯也属于稠环芳香烃.据此回答:
有两个或两个以上的苯环以共有环边的方式相互稠合的多环芳香烃称为稠环芳香烃.下图中椭圆烯也属于稠环芳香烃.据此回答:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 标准状况下,22.4 L CCl4含有4nA个Cl原子 | |
| B. | 7.8 g Na2O2与足量水反应转移0.2nA个电子 | |
| C. | 0.1 mol•L-1NaCl溶液中含有0.1nA个Na+ | |
| D. | 常温常压下,23 gNO2、N2O4混合气体中含有nA个氧原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 ;
;查看答案和解析>>
科目:高中化学 来源: 题型:解答题
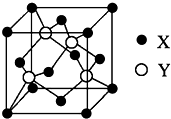 ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:
ⅥA族的氧、硫、硒(Se)、碲(Te)等元素在化合物中常表现出多种化合价,含ⅥA族元素的化合物在研究和生产中有许多重要用途.请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 直线形;平面三角形 | B. | V形;三角锥形 | ||
| C. | 直线形;三角锥形 | D. | V形;平面三角形 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 16.51 g | B. | 23.82 g | C. | 24.84 g | D. | 17.02 g |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 加入一定量C,平衡逆向移动 | |
| B. | 保持温度不变,容器容积压缩到原来的一半,物质B的浓度变为原来的1.8倍,则平衡正向移动 | |
| C. | 恒温恒压,再充入1mol氦气(不参与反应),A的转化率增大,则m<n | |
| D. | 恒温恒压,再加入2mol的A,气体的平均相对分子质量变为原来的2倍 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com