
| A、甲烷、乙烯和苯在工业上都可通过石油分馏得到 |
| B、米酒变酸的过程涉及了氧化反应 |
| C、乙烯和聚丙烯都能与氢气在一定条件下发生加成反应 |
| D、淀粉、葡萄糖、脂肪和蛋白质在一定条件下都能发生水解反应 |


科目:高中化学 来源: 题型:
 将CO2在一定条件下与H2反应转化为甲醇(CH4O)是变废为宝的好方法,一定条件下,每转化1kg CO2放出的热量为1113.64KJ,CO2转化为甲醇过程中浓度随时间的变化曲线如图所示(已知反应物和生成物在此条件下均为气体),下列叙述中正确的是( )
将CO2在一定条件下与H2反应转化为甲醇(CH4O)是变废为宝的好方法,一定条件下,每转化1kg CO2放出的热量为1113.64KJ,CO2转化为甲醇过程中浓度随时间的变化曲线如图所示(已知反应物和生成物在此条件下均为气体),下列叙述中正确的是( )| A、在进行到3分钟时,CO2和H2所表达的反应速率值相等,均为0.5mol?L-1?min-1 | ||
| B、此反应的热化学方程式为:CO2(g)+3H2(g)?CH4O(g)+H2O(g)△H=-49.0KJ/mol | ||
C、此条件下反应的平衡常数为
| ||
| D、降低温度,此反应的平衡常数可能为0.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在由水电离出的c(H+)=1×10-12mol/L的溶液中:Fe2+、ClO-、Na+、SO42- |
| B、c(OH-)=10-13mol?L-1的溶液中:SO32-、CO32-、Na+、K+ |
| C、在含有大量Fe3+的溶液中:Cu2+、Cl-、NO3-、S2- |
| D、加入Mg能放出H2的溶液中:K+、NH4+、Cl-、SO42- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、混合后溶液中存在有关系:C(K+)+C(Na+)+C(H+)=C(SO32-)+C(HSO3-)+C(OH-) |
| B、混合后溶液中存在有关系:C(K+)+C(H2SO3)+C(H+)=C(SO32-)+C(OH-) |
| C、混合后溶液中存在有关系:C(SO32-)+C(HSO3-)+C(H2SO3)=0.02 mol?L-1 |
| D、两溶液混合前,Na2SO3溶液中水电离出C(H+)小于KHSO3溶液中水电离出C(H+) |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
B、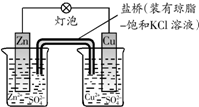 如图中电子由Zn极流向Cu,盐桥中的Cl-移向CuSO4溶液 |
| C、氢氧燃料电池(酸性电解质)中O2通入正极,电极反应为O2+4H++4e-═2H2O |
| D、电镀时,通常把待镀的金属制品作阳极 |
查看答案和解析>>
科目:高中化学 来源: 题型:
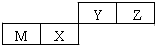
| A、原子半径Z>Y |
| B、X的最简单气态氢化物的热稳定性比Z的小 |
| C、Y的最高价氧化物对应水化物的酸性比X的弱 |
| D、M的最高价氧化物对应水化物不能与NaOH溶液反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| OH- |
| H- |
| c(HCO3-):c(H2CO3) | 1.0 | 17.8 | 20.0 | 22.4 |
| pH | 6.10 | 7.35 | 7.40 | 7.45 |
| A、pH=7的血液中,c(HCO3-)>c(H2CO3) |
| B、人体发生酸中毒时,可静脉滴注一定浓度的NaHCO3溶液解毒 |
| C、常温下将pH=7.40的血液稀释至pH=7时,c(H+)?c(OH-)一定不变 |
| D、c(HCO3-):c(H2CO3)=1时,H2CO3的电离程度小于HCO3-的水解程度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、冰熔化时水分子的共价键未发生断裂 |
| B、同族元素的氧化物形成的晶体类型相同 |
| C、分子晶体中,分子间作用力越大,分子越稳定 |
| D、具有高熔沸点的晶体一定是离子晶体或原子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
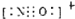
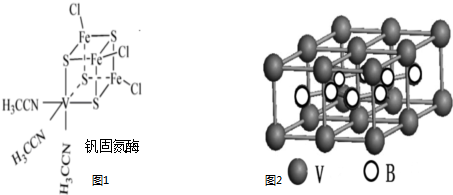
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com