
| t/s | 50 | 150 | 250 | 350 | |
| n(PCl3)/mol | 0.32 | 0.38 | 0.40 | 0.40 |
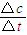 计算;
计算; =0.0016mol/(L?s),故B错误;
=0.0016mol/(L?s),故B错误;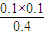 =0.025.
=0.025.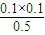 =0.02,K>Qc,说明平衡向正反应方向移动,反应达平衡前v(正)>v(逆),故C正确;
=0.02,K>Qc,说明平衡向正反应方向移动,反应达平衡前v(正)>v(逆),故C正确;

 教学练新同步练习系列答案
教学练新同步练习系列答案科目:高中化学 来源: 题型:
(2012?宜春模拟)温度为T时,向4L恒容密闭容器中充入2.0molPCl5,反应PCl5(g)?PCl3(g)+Cl2(g),经一段时间后达到平衡.反应过程中测定的部分数据见下表.
|
查看答案和解析>>
科目:高中化学 来源:宜春模拟 题型:单选题
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.32 | 0.38 | 0.40 | 0.40 |
| A.保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol?L-1,则反应的△H<0 |
| B.反应在前50s的平均速率v(PCl3)=0.0032 mol?L-1?s-1 |
| C.相同温度下,起始时向容器中充入2.0 mol PCl5、0.40 molPCl3和0.40 molCl2,反应达平衡前v(正)>v(逆) |
| D.相同温度下,起始时向容器中充入4.0 mol PCl3、和4.0 mol Cl2,达到平衡时,PCl3的转化率小于80% |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年四川省成都市高新区高三(上)期中化学试卷(解析版) 题型:选择题
| t/s | 50 | 150 | 250 | 350 | |
| n(PCl3)/mol | 0.32 | 0.38 | 0.40 | 0.40 |
查看答案和解析>>
科目:高中化学 来源:2012-2013学年辽宁省盘锦二中高三(上)第二次段考化学试卷(解析版) 题型:选择题
| t/s | 50 | 150 | 250 | 350 | |
| n(PCl3)/mol | 0.32 | 0.38 | 0.40 | 0.40 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com