
在强酸性溶液中,下列离子组能大量共存且溶液为无色透明的是
A.Na+、K+、OH-、Cl- B.Na+、Cu2+、SO42-、NO3-
C.Mg2+、Na+、SO42-、Cl- D.Ba2+、HCO3-、NO3-、K+
 孟建平名校考卷系列答案
孟建平名校考卷系列答案科目:高中化学 来源:2016届河北省高三上一轮收官考试理综化学试卷(解析版) 题型:选择题
下列解释事实的化学方程式或离子方程式不正确的是( )
A.向海带灰浸出液中加入硫酸、双氧水:2I-+2H++H2O2=I2+2H2O
B.自然界各种原生铜的硫化物经氧化、淋滤作用后产生的硫酸铜,遇到难溶液的PbS,慢慢转变为铜蓝(CuS):Cu2++SO42-+PbS═CuS+PbSO4
C.在燃煤时加入适量石灰石,可减少SO2的排放:2CaCO3+O2+2SO2═2CaSO3+2CO2
D.在盐碱地(含较多NaCl、Na2CO3)上通过施加适量CaSO4,可降低土壤的碱性:CaSO4+Na2CO3═CaCO3↓+Na2SO4
查看答案和解析>>
科目:高中化学 来源:2015-2016学年广东汕头金山中学高二上10月月考化学卷(解析版) 题型:填空题
物质A是生产各种塑料的重要单体,工业上采用物质B分解制备物质A的同时释放出氢气,其制备原理是:B(g) A(g)+H2(g) ΔH=+125kJ·mol—1
A(g)+H2(g) ΔH=+125kJ·mol—1
(1)该反应的平衡常数表达式为K=______________。随着温度的升高,K 值____________ (填“增大”、“减小”或“不变”)。
(2)实际生产中常以高温水蒸气作为反应体系的稀释剂(稀释剂不参加反应)。物质B的平衡转化率与水蒸气的用量、体系总压强关系如下图。

①由上图可得出:
结论一:
其他条件不变,水蒸气的用量越大,平衡转化率越___;
结论二 :______________________________________
②加人稀释剂能影响反应物B的平衡转化率的原因是:__________________。
(3)某些工艺中,在反应的中途加入O2和特定的催化剂,有利于提高B的平衡转化率。试解释其原因:________________________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上二调考试化学试卷(解析版) 题型:选择题
室温下向10mLpH=3的醋酸溶液中加水稀释后,下列说法正确的是( )
A.溶液中导电粒子的数目减少
B.溶液中c(CH3COO?) /c(CH3COOH)•c(OH?) 不变
C.醋酸的电离程度增大,c(H+)亦增大
D.再加入10mLpH=11的NaOH溶液,混合液的pH=7
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上期中(理)化学试卷(解析版) 题型:选择题
对于可逆反应:2A(g)+B(g) 2C(g) △H<0。下列与该反应相关的各图中,正确的是
2C(g) △H<0。下列与该反应相关的各图中,正确的是
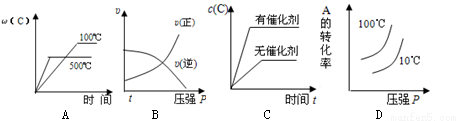
查看答案和解析>>
科目:高中化学 来源:2015-2016学年江西省高二上二次月考化学试卷(解析版) 题型:填空题
由于温室效应和资源短缺等问题,如何降低大气中的CO2含量并加以开发利用,引起了各国的普遍重视。目前工业上有一种方法是用CO2生产燃料甲醇。一定条件下发生反应:CO2(g)+3H2(g) CH3OH(g)+H2O(g),右图表示该反应进行过程中能量的变化。
CH3OH(g)+H2O(g),右图表示该反应进行过程中能量的变化。
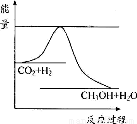
(1)关于该反应的下列说法中,正确的是_______。
A.△H>0,△S>0; B.△H>0,△S<0;
C.△H<0,△S<0; D.△H<0,△S>0。
(2)该图中能量的最高点和最低点之间的差值代表
(3)以CH4和H2O为原料,通过下列反应来制备甲醇。
①CH4(g)+H2O(g) == CO(g)+3H2(g) △H=+206.0KJ/mol
②CO(g) + 2H2(g) = CH3OH(g) △H=-129.0KJ/mol
CH4(g)和H2O(g)反应生成CH3OH(g)和H2(g)的热化学方程式为 。
查看答案和解析>>
科目:高中化学 来源:2016届浙江省高三上学期期中考试化学试卷(解析版) 题型:选择题
臭氧是理想的烟气脱硝试剂,其脱硝反应为2NO2(g)+O3(g)  N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
N2O5(g)+O2(g),若反应在恒容密闭容器中进行,下列由该反应相关图像作出的判断正确的是
A | B | C | D |
|
|
|
|
0~3s内,反应速率v(O3)=0.2mol·L-1·s-1 | 降低温度,平衡常数增大 | t1时仅加入催化剂,平衡正向移动 | 达平衡时,仅改变x,则x为c(O2) |
查看答案和解析>>
科目:高中化学 来源:2016届浙江绍兴市高三上学期期中考试化学试卷(解析版) 题型:选择题
原子序数依次增大的X、Y、Z、W四种短周期元素,X、W原子的最外层电子数与其电子层数相等,X、Z的最外层电子数之和与Y、W的最外层电子数之和相等。甲的化学式为YX3,是一种刺激性气味的气体,乙的化学式为YZ3,丙是由X、Y、Z组成的盐。下列说法正确的是
A.原子半径:W>Y>Z,而离子半径: Z>Y>W
B.化合物丙中只存在共价键
C.测得丙的水溶液呈酸性,则溶液中丙盐阳离子浓度大于酸根离子浓度
D.甲沸点远高于乙,可能是甲分子间存在氢键所致
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上学期期中考试化学试卷(解析版) 题型:选择题
工业生产中物质的循环利用有多种,例如:
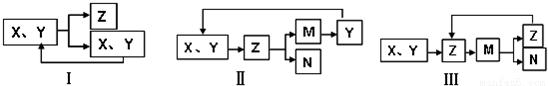
下列表示不正确的是
A.图Ⅰ可表示合成氨,其中N2、H2被循环使用
B.图Ⅱ可表示电解熔融的MgCl2得到镁,其中HCl循环使用
C.图Ⅲ可表示氨催化氧化法制硝酸,其中NO循环使用
D.图Ⅰ可用于侯氏制纯碱CO2的循环利用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com