
【题目】
化合物M是合成香精的重要原料。实验室由A和芳香烃E制备M的一种合成路线如下:
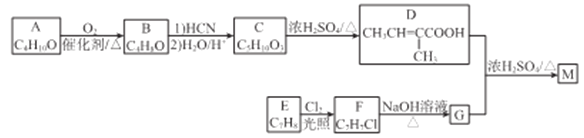
已知: (R1、R2表示烃基或H原子)
(R1、R2表示烃基或H原子)
请回答下列题:
(1)A的化学名称为_________,B的结构简式为________。
(2)C中官能团的名称为________。
(3)D分子中最多有___个原子共平面。
(4)E→F的反应类型为________。
(5)D+G→M的化学方程式为________。
(6)同时满足下列条件的D的同分异构体有___种(不考虑立体异构),其中核磁共振氢谱有3组峰的结构简式为________。
①能发生水解反应和银镜反应; ②不含环状结构
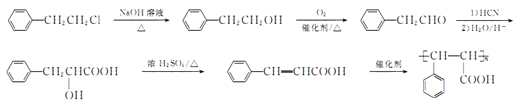
(7)参照上述合成路线和信息。以![]() 为原料(其他无机试剂任选),设计制备
为原料(其他无机试剂任选),设计制备 的合成路线_______________________。
的合成路线_______________________。
【答案】 2-丁醇 ![]() 羟基、羧基 11 取代反应
羟基、羧基 11 取代反应 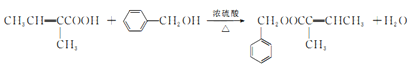 8
8 ![]()
【解析】由题中信息可以推知,A为![]() ,发生催化氧化生成B,B为
,发生催化氧化生成B,B为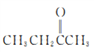 ,B与HCN发生加成反应后再水解生成C,C为
,B与HCN发生加成反应后再水解生成C,C为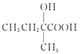 ,C发生消去反应生成D,由E的分子式可知,E为
,C发生消去反应生成D,由E的分子式可知,E为![]() ,与氯气在光照条件下发生取代反应生成F,F为
,与氯气在光照条件下发生取代反应生成F,F为![]() ,F发生水解反应生成G,G为
,F发生水解反应生成G,G为![]() ,G与D发生酯化反应生成M,M为
,G与D发生酯化反应生成M,M为 。
。
(1). A的化学名称为2-丁醇,B的结构简式为![]() ,故答案为:2-丁醇;
,故答案为:2-丁醇;![]() ;
;
(2). 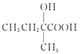 中官能团的名称为羟基、羧基,故答案为:羟基、羧基;
中官能团的名称为羟基、羧基,故答案为:羟基、羧基;
(3). 根据碳碳双键和碳氧双键为平面结构,![]() 分子中最多有11个原子共平面,故答案为:11;
分子中最多有11个原子共平面,故答案为:11;
(4). ![]() 和氯气在光照条件下发生取代反应生成
和氯气在光照条件下发生取代反应生成![]() ,故答案为:取代反应;
,故答案为:取代反应;
(5). ![]() 和
和![]() 发生酯化反应的化学方程式为:
发生酯化反应的化学方程式为: ,故答案为:
,故答案为: ;
;
(6). D为![]() ,由信息可知其同分异构体属于甲酸酯,则先写出C4H8属于烯烃的同分异构体有:CH2CHCH2CH3、CH3CH=CHCH3、CH2=C(CH3)2,共3种,再用HCOO-取代各烯烃中不同化学环境的H原子,CH2=CHCH2CH3有4种取代方式,CH3CH=CHCH3有2种取代方式,CH2=C(CH3)2有2种取代方式,共有8种同分异构体,其中核磁共振氢谱有3组峰的结构简式为
,由信息可知其同分异构体属于甲酸酯,则先写出C4H8属于烯烃的同分异构体有:CH2CHCH2CH3、CH3CH=CHCH3、CH2=C(CH3)2,共3种,再用HCOO-取代各烯烃中不同化学环境的H原子,CH2=CHCH2CH3有4种取代方式,CH3CH=CHCH3有2种取代方式,CH2=C(CH3)2有2种取代方式,共有8种同分异构体,其中核磁共振氢谱有3组峰的结构简式为![]() ,故答案为:8;
,故答案为:8;![]() ;
;
(7). ![]() 发生水解反应生成
发生水解反应生成![]() ,再发生氧化反应生成
,再发生氧化反应生成![]() ,进一步与HCN加成后水解得
,进一步与HCN加成后水解得![]() ,该物质发生消去反应得
,该物质发生消去反应得![]() ,最后发生加聚反应得目标产物,则合成路线为:
,最后发生加聚反应得目标产物,则合成路线为: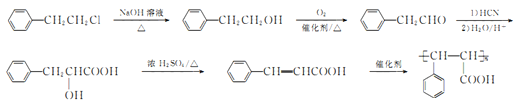 ,故答案为:
,故答案为: 。
。


科目:高中化学 来源: 题型:
【题目】关于有机物a(![]() )、b(
)、b(![]() )、c(
)、c(![]() )的说法正确的是
)的说法正确的是
A. a、b、c的分子式均为C8H8
B. a、b、c均能与溴水发生反应
C. a、b、c中只有a的所有原子会处于同一平面
D. a、b、c的一氯代物中,b有1种,a、c均有5种(不考虑立体异构)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列分子或离子①F- ②Na+ ③HF ④NH3⑤CH4其中与氖原子含有相同电子数的是( )
A. ①②③ B. ②③④ C. ①②⑤ D. ①②③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】NH3作为一种重要化工原料,被大量应用于工业生产,与其有关性质反应的催化剂研究曾被列入国家863计划。催化剂常具有较强的选择性,即专一性。已知:
反应I:4NH3(g) +5O2(g)![]() 4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
4NO(g) +6H2O(g) △H=―905.0 kJ·molˉ1
反应 II:4NH3(g)+3O2(g)![]() 2N2(g) +6H2O(g) △H
2N2(g) +6H2O(g) △H
(1)
化学键 | H—O | O=O | N≡N | N—H |
键能kJ·molˉ1 | 463 | 496 | 942 | 391 |
△H=__________________ 。
(2)在恒温恒容装置中充入一定量的NH3和O2,在某催化剂的作用下进行反应I,则下列有关叙述中正确的是__________________。
A.使用催化剂时,可降低该反应的活化能,加快其反应速率
B.若测得容器内4v正(NH3)=6v逆(H2O)时,说明反应已达平衡
C.当容器内![]() =1时,说明反应已达平衡
=1时,说明反应已达平衡
(3)氨催化氧化时会发生上述两个竞争反应I、II。为分析某催化剂对该反应的选择性,在1L密闭容器中充入1 mol NH3和2mol O2,测得有关物质的量关系如下图:
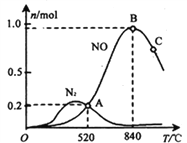
①该催化剂在高温时选择反应____________ (填“ I ”或“ II”)。
② 520℃时,4NH3(g)+5O2![]() 4NO(g) +6H2O(g)的平衡常数K=____________________________ (不要求得出计算结果,只需列出数字计算式)。
4NO(g) +6H2O(g)的平衡常数K=____________________________ (不要求得出计算结果,只需列出数字计算式)。
③有利于提高NH3转化为N2平衡转化率的措施有_______________
A.使用催化剂Pt/Ru
B.使用催化剂Cu/TiO2
C.增大NH3和O2的初始投料比
D.投料比不变,增加反应物的浓度
E.降低反应温度
(4)采用氨水吸收烟气中的SO2,
①若氨水与SO2恰好完全反应生成正盐,则此时溶液呈_____性(填“酸”或“碱”)常温下弱电解质的电离平衡常数如下:氨水:Kb=1.8×10ˉ5mol·Lˉ1;H2SO3 :Ka1=1.3×10ˉ2mol·Lˉ1,Ka2=6.3×10ˉ8mol·Lˉ1
②上述溶液中通入______气体可使溶液呈中性,(填“SO2”或NH3”)此时溶液离子浓度由大到小的顺序_________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某小组对碳与浓硝酸的反应进行探究,已知:2NaOH+2NO2=NaNO3+NaNO2+H2O,2NaOH+NO2+NO=2NaNO2+H2O。请回答下列可题:
I.甲同学设计 如图所示装置制备并收集NO
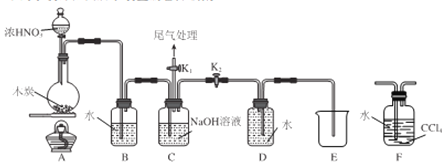
(1)碳与浓硝酸反应的化学方程式为__________________。
(2)C的作用为_______________。
(3)乙同学认为用装置F代替B更合理,理由为_______________。
(4)乙同学用改进后的装置进行实验。
①将浓HNO3滴入圆底烧瓶中的操作为__________________。
②点燃A处酒精灯开始反应后,圆底烧瓶中的现象为________________。
II.探究NO与Na2O2反应
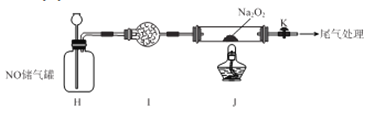
已知NaNO2既有氧化性,又有还原性;J 处硬质玻璃管中制得的NaNO2中含有少量NaNO3。
(5)检验上图装置气密性的方法为____________________。
(6)实验结束后,设计实验证明J 处硬质玻璃管中有NaNO2生成________________。
供选试剂:蒸馏水KI-淀粉溶液,KMnO4溶液、NaOH溶液.BaCl2溶液、稀硫酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作正确的是( )
A.用托盘天平称取1.06gNa2CO3固体
B.用10mL量筒量取8.58mL蒸馏水
C.用稀盐酸洗净做焰色反应的铁丝
D.为了加快过滤的速率,用玻璃搅拌过滤器中的溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)1780年,意大利解剖学家伽伐尼在用银质手术刀触碰放在铁盘上的青蛙时,无意间发现青蛙腿部肌肉抽搐了一下,仿佛受到电流的刺激。伽伐尼认为出现这种现象的原因是动物体内存在“生物电”。结合你所学的知识模拟该过程,下列哪种材质的手术刀触碰铁盘上的青蛙腿不会产生触动_________(填字母)。
a、铝 b、玻璃 c、银 d、铁
(2)1799年,伏打仔细研究了伽伐尼的发现,以含食盐水的湿抹布,夹在银和锌的圆形版中间,堆积成圆柱状,制造出世界上最早的电池-伏打电池。将洁净的金属片A、B、D、E分别放置在浸有盐溶液的滤纸上面并压紧(如下图所示)。在每次实验时,记录电压表指针的移动方向和电压表的读数如下:
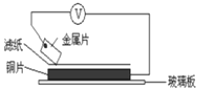
金属 | 电子流动方向 | 电压(V) |
A | A→Cu | +0.78 |
B | Cu→B | -0.15 |
D | D→Cu | +1.35 |
E | E→Cu | +0.30 |
已知:构成两电极的金属其金属活泼性相差越大,电压表的读数越大。请依据表中数据判断:_______金属可能是最强的还原剂;______金属一定不能从硫酸铜溶液中置换出铜。
(3)1836年,英国科学家丹尼尔对伏打电池进行改进,获得了世界上第一个具有稳定电流的电池,下图是丹尼尔电池的简易装置:
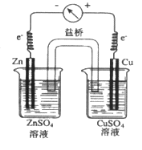
该电池的正极反应是_____________,负极反应 __________。
(4)随着社会的发展和科技的进步,越来越多的电池被制造出来。请选择适宜的材料和试剂设计一个原电池,使它的正极反应为:Fe3++e-=Fe2+以“![]() ”代表反应容器,“
”代表反应容器,“![]() ”代表导线,“
”代表导线,“![]() ”代表电极,“
”代表电极,“![]() ”代表小灯泡,
”代表小灯泡,
在下图方框内画出装置图并指出电极材料和电解质溶液,标出电源的正负极________。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是某核苷酸与核苷酸长链的示意图,据图回答问题:

(1)已知图甲的分子结构式右上角的含氮碱基为腺嘌呤(A)。请观察后回答下列问题:
图甲所示的核苷酸的名称是_________。该核苷酸是构成______的原料。
(2)图乙为一条核苷酸长链的片段,据图回答:
①图中所示1、2、3的名称分别是___、___、_____。4、5的名称分别是__、__。
②此结构中与另一种核酸相比较,其特有的碱基中文名称是_________。
(3)将水稻根细胞中的遗传物质彻底水解后,可得到
A.一种五碳糖B.四种脱氧核糖核苷酸C.5种含氮碱基D.8种核苷酸
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com