
| 实验目的 | 实验操作 | |
| A | 制备Fe(OH)3胶体 | 将饱和的FeCl3溶液滴加到NaOH浓溶液中 |
| B | 由MgCl2溶液制备无水MgCl2 | 将MgCl2溶液加热蒸干,趁热过滤 |
| C | 除去HBr中混有的Br2 | 将混合气通入盛有CCl4的洗气瓶 |
| D | 证明Cu(OH)2的溶度积比Mg(OH)2的小 | 将1mL0.1mol•L-1MgSO4溶液逐滴滴入4mL0.1mol•L-1NaOH溶液,再滴加1mL0.1mol•LCuSO4溶液 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.氯化铁与氢氧化钠溶液反应生成的氢氧化铁沉淀,不是胶体;
B.氯化氢易挥发,蒸干氯化镁溶液得到的是氢氧化镁沉淀;
C.溴易溶于四氯化碳,而HBr不溶;
D.氢氧化钠过量,无法据此比较氢氧化铜、氢氧化镁的溶度积.
解答 解:A.将饱和的FeCl3溶液滴加到NaOH浓溶液中生成氢氧化铁沉淀,无法制备氢氧化铁胶体,故A错误;
B.将MgCl2溶液加热蒸干,由于HCl易挥发,得到的是氢氧化镁沉淀,应该在HCl气流中加热制备无水MgCl2,故B错误;
C.HBr不溶于四氯化碳,而溴单质易溶于四氯化碳,将混合气通入盛有CCl4的洗气瓶,可除去HBr中混有的Br2,故C正确;
D.将1mL0.1mol•L-1MgSO4溶液逐滴滴入4mL0.1mol•L-1NaOH溶液,氢氧化钠过量,无法据此比较Cu(OH)2、Mg(OH)2的溶度积大小,故D错误;
故选C.
点评 本题考查了化学实验方案的评价,题目难度中等,涉及盐的水解原理、胶体制备、溶度积大小比较、物质分离与提纯等知识,明确氢氧化铁胶体制备方法、盐的水解原理为解答关键,试题培养了学生的分析能力及灵活应用能力.


 挑战100单元检测试卷系列答案
挑战100单元检测试卷系列答案科目:高中化学 来源: 题型:解答题
| 操作 | 现象 | 结论 |
| 取少量溶液于试管中,加入KSCN溶液,振荡 | ①颜色无变化 | 不存在Fe3+ |
| 另取少量溶液于试管中,加入②K3[Fe(CN)6]溶液,振荡 | 蓝色沉淀 | 存在Fe2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
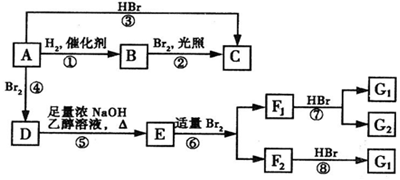
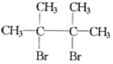 ,F1和F2互为同分异构体,G1和G2互为同分异构体.)
,F1和F2互为同分异构体,G1和G2互为同分异构体.)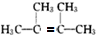 .
.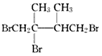 .
.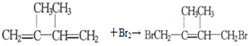 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
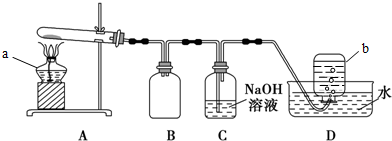
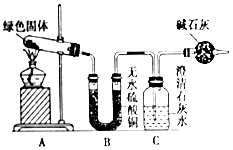 铜器久置,表面会生成一层绿色固体,某化学兴趣小组收集家中铜器表面的绿色固体进行探究.查阅相关资料后,得知该绿色物质是碱式碳酸铜.该小组同学利用如图装置进行实验,探究碱式碳酸铜的分解产物.
铜器久置,表面会生成一层绿色固体,某化学兴趣小组收集家中铜器表面的绿色固体进行探究.查阅相关资料后,得知该绿色物质是碱式碳酸铜.该小组同学利用如图装置进行实验,探究碱式碳酸铜的分解产物.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 反应2CO(g)=2C(s)+O2(g)△H>0可以自发进行 | |
| B. | 放热反应在常温条件下一定很容易进行 | |
| C. | 平衡常数发生变化,化学平衡一定发生移动 | |
| D. | 化学平衡发生移动,平衡常数一定发生改变 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 10 mL 0.5 mol/L CH3COONa溶液与6 mL 1 mol/L盐酸混合:c(Cl-)>c(Na+)>c(OH-)>c(H+) | |
| B. | 0.1 mol/L pH为4的NaHB溶液中:c(HB-)>c(H2B)>c(B2-) | |
| C. | 在NaHA溶液中一定有:c(Na+)+c(H+)=c(HA-)+c(OH-)+c(A2-) | |
| D. | c(NH4+)相等的(NH4)2SO4溶液、(NH4)2CO3溶液和NH4Cl溶液:c[(NH4)2SO4]<c[(NH4)2CO3]<c(NH4Cl) |
查看答案和解析>>
科目:高中化学 来源: 题型:推断题
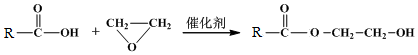
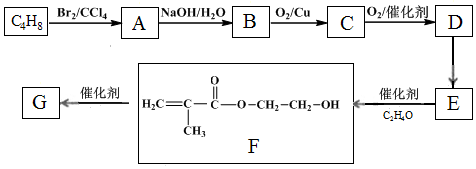
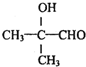 .
.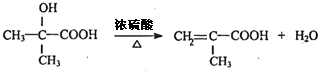 .
.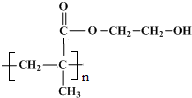 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com