
(1)已知:H2(g)+1/2O2(g)=H2O(l) ΔH=-285.8 kJ·mol-1
H2(g)=H2(l) ΔH=-0.92 kJ·mol-1
O2(g)=O2(l) ΔH=-6.84 kJ·mol-1
H2O(l)=H2O(g) ΔH=+44.0 kJ·mol-1
请写出液氢和液氧反应生成气态水的热化学方程式:__________________________
电解质溶液为KOH溶液的氢氧燃料电池,其负极的电极反应式为____________________________________。
(2)如图表示373 K时,反应A(g) 2B(g)在前110 s内的反应进程。
2B(g)在前110 s内的反应进程。
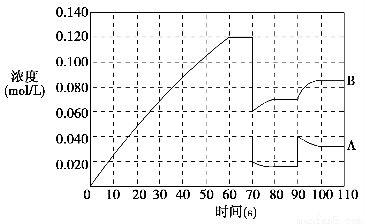
①此反应的平衡常数表达式K=________。
②373 K时反应进行到70 s时,改变的条件可能是________,反应进行到90 s时,改变的条件可能是________。
A.加入催化剂 B.扩大容器体积 C.升高温度 D.增大A的浓度
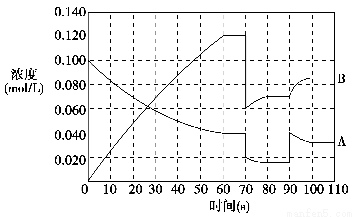
③请在图中画出反应物A在0~70 s时的浓度变化曲线。
(1)H2(l)+1/2O2(l)=H2O(g) ΔH=-237.46 kJ·mol-1
H2+2OH--2e-=2H2O
(2)①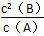 ②B D ③如图
②B D ③如图
【解析】 本题综合考查化学反应原理内容,考查了盖斯定律的应用、化学平衡的移动、电极反应式的书写等知识,意在考查考生运用化学原理解决问题的能力。
(1)由盖斯定律,利用题给的热化学反应方程式推导可得要求的热化学方程式为H2(l)+1/2O2(l)=H2O(g) ΔH=-237.46 kJ·mol-1。
(2)②反应进行到70 s时B的浓度和A的浓度均降低为原来的1/2,且平衡移动时B的浓度逐渐增大,A的浓度逐渐减小,即平衡向右移动,可以判断改变的条件是扩大容器体积。反应进行到90 s时A的浓度突然增大,平衡移动时A的浓度逐渐变小,B的浓度逐渐变大,即平衡向右移动,可以判断改变的条件是增大A的浓度。③由图可以看出反应起始时B的浓度为0,进行到60 s时达到平衡状态,此时A的浓度为0.040 mol·L-1,B的浓度为
0.120 mol·L-1,由化学计量数关系知B的浓度变化量是A的浓度变化量的2倍,可以求出A的起始浓度为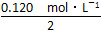 +0.040 mol·L-1=0.100 mol·L-1,可以画出对应曲线。
+0.040 mol·L-1=0.100 mol·L-1,可以画出对应曲线。


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2014年高一下学期化学必修2 1-1-3 核素练习卷(解析版) 题型:选择题
在11 g由D和18O组成的水中,含中子数为(NA表示阿伏加德罗常数)( )。
A.NAB.2NAC.6NAD.10NA
查看答案和解析>>
科目:高中化学 来源:2014年江苏省南通市业水平测试(必修)化学试卷(解析版) 题型:选择题
氢氧燃料电池可以使用在航天飞机上,其反应原理示意图如右图。下列有关氢氧燃料电池的说法不正确的是

A.该电池工作时化学能转化为电能
B.该电池中电极b是正极,发生还原反应
C.外电路中电流由电极a通过导线流向电极b
D.该电池的总反应:2H2+O2=2H2O
查看答案和解析>>
科目:高中化学 来源:2014年江苏省南通市业水平测试(必修)化学试卷(解析版) 题型:选择题
下列说法正确的是
A.石墨是电解质 B.干冰是氧化物
C.铝热剂是纯净物 D.冰醋酸是混合物
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练四 氧化还原反应的规律与应用练习卷(解析版) 题型:选择题
硫氰(SCN)2的化学性质和卤素(X2)类似,称为拟卤素,如(SCN)2+H2O HSCN+HSCNO,它们阴离子的还原性强弱为Cl-<Br-<SCN-<I-,下列说法不正确的是( )
HSCN+HSCNO,它们阴离子的还原性强弱为Cl-<Br-<SCN-<I-,下列说法不正确的是( )
A.Cl2可以与KSCN溶液反应
B.(SCN)2可以与KI溶液反应
C.KSCN溶液可以与FeCl3溶液反应
D.(SCN)2可以与KBr溶液反应
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十八 探究型综合实验题练习卷(解析版) 题型:实验题
资料显示:镁与饱和碳酸氢钠溶液反应产生大量气体和白色不溶物。某同学设计了如下实验方案并验证产物、探究反应原理。
(1)提出假设
实验Ⅰ:用砂纸擦去镁条表面氧化膜,将其放入盛有适量滴有酚酞的饱和碳酸氢钠溶液的试管中,迅速反应,产生大量气泡和白色不溶物,溶液由浅红变红。
该同学对反应中产生的白色不溶物做出如下猜测:
猜测1:白色不溶物可能为________________。
猜测2:白色不溶物可能为MgCO3。
猜测3:白色不溶物可能是碱式碳酸镁[xMgCO3·yMg(OH)2]。
(2)设计定性实验确定产物并验证猜测:
实验序号 | 实验 | 实验现象 | 结论 |
实验Ⅱ | 将实验Ⅰ中收集到的气体点燃 | 能安静燃烧、产生淡蓝色火焰 | ①气体成分为________ |
实验Ⅲ | ②取实验Ⅰ中的白色不溶物,洗涤,加入足量________ | ③________________ __________________ __________________ | 白色不溶物可能含有MgCO3 |
实验Ⅳ | 取实验Ⅰ中的澄清液,向其中加入少量CaCl2稀溶液 | 产生白色沉淀 | ④溶液中存在________ |
(3)为进一步确定实验Ⅰ的产物,设计定量实验方案,如图所示:

称取实验Ⅰ中所得干燥、纯净的白色不溶物22.6 g,充分加热至不再产生气体为止,并使分解产生的气体全部进入装置A和B中。实验后装置A增重1.8 g,装置B增重8.8 g,试确定白色不溶物的化学式:__________________________ ______________________________________________。
(4)请结合化学用语和化学平衡移动原理解释Mg和饱和NaHCO3溶液反应产生大量气泡和白色不溶物的原因:____________________________________。
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十五 常见仪器的使用及实验基本操作练习卷(解析版) 题型:选择题
除去下列物质中所含杂质(括号内为杂质),选用的试剂或分离方法正确的是( )。
混合物试剂分离方法
AFe(碘)—加热
B二氧化碳(氯化氢)饱和Na2CO3溶液洗气
C乙酸乙酯(乙酸)NaOH溶液蒸馏
D淀粉(氯化钠)蒸馏水渗析
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练十三 有机物结构及同分异构体数目判断练习卷(解析版) 题型:选择题
下列有关说法正确的是 ( )。
A.丙烯的结构简式为CH2CHCH3
B.2,2-二甲基丙烷的一氯代物有2种
C.分子式为CH4O和C2H6O的物质一定互为同系物
D.键线式为 的有机物的分子式为C8H8
的有机物的分子式为C8H8
查看答案和解析>>
科目:高中化学 来源:2014年化学高考题型专练五 元素周期表中位-构-性关系的分析练习卷(解析版) 题型:选择题
甲、乙、丙、丁、戊是中学化学常见的无机物,其中甲、乙均为单质,它们的转化关系如图所示(某些条件和部分产物已略去)。下列说法不正确的是
( )。
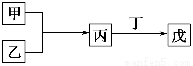
A.若组成甲、乙的元素位于同一周期,则戊可能是一种弱酸
B.若组成甲、乙的元素位于同一主族,则戊可能是一种弱酸
C.若甲为短周期中原子半径最大的主族元素形成的单质,且戊为碱,则丙只能为Na2O2
D.若丙、丁混合生成白烟,且丙为18电子分子,丁为10电子分子,则乙的水溶液可能具有漂白作用
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com