
用右图所示装置除去含CN-、Cl-废水中的CN-时,控制溶液pH为9~10,阳极产生的ClO-将CN-氧化为两种无污染的气体。下列说法不正确的是

A.用石墨作阳极,铁作阴极
B.阳极的电极反应式:Cl-+2OH--2e-===ClO-+H2O
C.阴极的电极反应式:2H2O+2e-===H2↑+2OH-
D.除去CN-的反应:2CN-+5ClO-+2H+===N2↑+2CO2↑+5Cl-+H2O
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源:2017届湖北省高三上学期8月月考化学试卷(解析版) 题型:选择题
一定条件下,在密闭容器里进行如下可逆反应:S2Cl2(橙黄色液体)+Cl2(气)  2SCl2(鲜红色液体)△H=-61.16kJ·mol-1。下列说法正确的是
2SCl2(鲜红色液体)△H=-61.16kJ·mol-1。下列说法正确的是
A.单位时间里生成n mol S2Cl2的同时也生成n mol SCl2
B.达到平衡时,若升高温度,压强不变,氯气转化率增大
C.达到平衡时,单位时间里消耗 n mol S2Cl2的同时也生成n molCl2
D.加入氯气,平衡向正反应方向移动,氯气的转化率一定升高
查看答案和解析>>
科目:高中化学 来源:2017届江西省高三上学期第二次月考化学试卷(解析版) 题型:选择题
已知:Fe(OH)3和Al(OH)3沉淀的生成与溶解的pH如下表。
氢氧化物 | 溶液pH | |||
开始沉淀 | 沉淀完全 | 沉淀开始溶解 | 沉淀完全溶解 | |
Fe(OH)3 | 2.3 | 3.4 | —— | —— |
Al(OH)3 | 3.3 | 5.2 | 7.8 | 12.8 |
向FeCl3、Al2(SO4)3的混合溶液中逐滴加入Ba(OH)2溶液,形成沉淀的情况如下图所示。以下推断错误的是

A.AB段可能发生的反应:2Ba2++3OH-+2SO42-+Al3+=2BaSO4↓+Al(OH)3↓
B.C点对应的沉淀:Fe(OH)3和BaSO4
C.OA段可能发生的反应:3Ba2++6OH-+3SO42-+Al3++Fe3+=3BaSO4↓+Fe(OH)3↓+Al(OH)3↓
D.据图计算原溶液中:c(Cl-)=c(SO42-)
查看答案和解析>>
科目:高中化学 来源:2017届湖北省沙市高三上学期第三次考试化学试卷(解析版) 题型:实验题
铝镁合金已成为飞机制造、化工生产等行业的重要材料.研究性学习小组的同学,为测定某含镁3%-5%的铝镁合金(不含其它元素)中镁的质量分数,设计下列两种不同实验方案进行探究.填写下列空白.
【方案一】
【实验方案】将铝镁合金与足量NaOH溶液反应,测定剩余固体质量。
实验中发生反应的化学方程式是__________.
【实验步骤】
(1)称取10.8g铝镁合金粉末样品,溶于V mL 物质的量浓度为4.0mol/L NaOH溶液中,充分反应。则NaOH溶液的体积V≥______mL。
(2)过滤、洗涤、干燥、称量固体.该步骤中若未洗涤固体,测得镁的质量分数将__________(填“偏高”、“偏低”或“无影响”).
【方案二】
【实验方案】将铝镁合金与足量稀硫酸溶液反应,测定生成气体的体积.
【实验步骤】
(1)同学们拟选用下列实验装置完成实验:

你认为最简易的装置其连接顺序是:A→( )→( )→( )→( )→( )(填接口字母,可不填满)。
(2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸 滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接广口瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了如图所示的实验装置。

①与前面(1)中装置相比该装置中导管a的作用有 .
②实验中将碱式滴定管改装成量气管,且实验前后量气管中液面读数分别为V1 mL、V2 mL.则产生氢气的体积为__________mL。
③若需确定产生氢气的物质的量,还需测定的数据是 。
查看答案和解析>>
科目:高中化学 来源:2017届湖北省沙市高三上学期第三次考试化学试卷(解析版) 题型:选择题
X、Y、Z、W为四种短周期主族元素,且原子序数依次增大,其中X、Z同族,Y是短周期主族元素中原子半径最大的,X是农作物生长的三种必须营养元素之一,W的单质以前常用于自来水消毒。下列说法正确的是
A. Z的最高价氧化物的水化物能形成多种含Y元素的盐
B. W的氧化物对应水化物的酸性一定强于Z
C. Y的单质应该保存在水中
D. X的氢化物沸点比Z的氢化物沸点低
查看答案和解析>>
科目:高中化学 来源:2017届湖北省沙市高三上学期第三次考试化学试卷(解析版) 题型:选择题
下列关于含硫化合物的叙述不正确的是
A.SO2能与CaO反应,可用生石灰作工业废气的脱硫剂
B.SO2能使碘的淀粉溶液由蓝色变为无色,体现出漂白性
C.浓硫酸和Na2SO3反应制取SO2时,浓硫酸只表现酸性
D.医疗上曾用硫酸钡作X射线透视肠胃的内服药剂
查看答案和解析>>
科目:高中化学 来源:2017届海南省高三上学期第一次月考化学试卷(解析版) 题型:推断题
I、下列说法正确的是( )
A.已知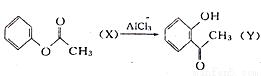 ,X与Y互为同分异构体,可用FeCl3溶液鉴别
,X与Y互为同分异构体,可用FeCl3溶液鉴别
B. 能发生的反应类型:加成反应、取代反应、消去反应、水解反应
能发生的反应类型:加成反应、取代反应、消去反应、水解反应
C.3-甲基-3-乙基戊烷的一氯代物有3种
D.相同条件下乙酸乙酯在水中的溶解度比其在乙醇中的溶解度大
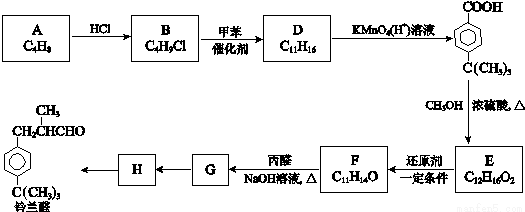
II、铃兰醛具有甜润的香味,常用作肥料、洗涤剂和化妆品的香料。合成铃兰醛的路线如下图所示(部分试剂和条件未注明):
已知: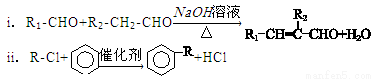
请回答:
(1)由A生成B的反应类型是______________。
(2)D的结构简式是______________。
(3)生成E的化学方程式是_____________。
(4)F能发生银镜反应,F的结构简式是________________。
(5)下列有关G的叙述中,不正确的是________________(填字母)。
A.G分子中有四种不同化学环境的氢原子
B.G能发生加聚反应、氧化反应和还原反应
C.1molG 最多能与4molH2发生加成反应
(6)由H生成铃兰醛的化学方程式是______________。
(7)F向G转化的过程中,常伴有分子式为C17H22O的副产物K产生。K的结构简式是____________。
查看答案和解析>>
科目:高中化学 来源:2017届海南省高三上学期第一次月考化学试卷(解析版) 题型:选择题
下列物质中属于高分子化合物的是( )
①淀粉②纤维素 ③氨基酸④油脂 ⑤蔗糖 ⑥酚醛树脂 ⑦聚乙烯⑧蛋白质
A.①②③⑦⑧ B.①④⑥⑦ C.①②⑥⑦⑧ D.②③④⑥⑦⑧
查看答案和解析>>
科目:高中化学 来源:2017届福建省高三上适应性考试(一)理综化学试卷(解析版) 题型:填空题
氨是生产硝酸、尿素等物质的重要原料,工业合成氨是最重要的化工生产之一。
(1)氨催化氧化法是工业制硝酸的主要方法。
已知:2NO(g)+3H2(g) 2NH3(g)+O2(g) △H1=-272.9 kJ·mol-1, 2H2(g)+O2(g)═2H2O(g) △H2= -483.6kJ·mol-1,则4NH3(g)+5O2(g)=4NO(g)+ 6H2O(g)△H3= 。
2NH3(g)+O2(g) △H1=-272.9 kJ·mol-1, 2H2(g)+O2(g)═2H2O(g) △H2= -483.6kJ·mol-1,则4NH3(g)+5O2(g)=4NO(g)+ 6H2O(g)△H3= 。
(2)恒容密闭容器中进行合成氨反应N2(g) +3H2(g)  2NH3(g) △H4 = - 92. 4 kJ·mol-1,
2NH3(g) △H4 = - 92. 4 kJ·mol-1,
ΔS=-198.2J?mol-1?K-1。其化学平衡常数(K)与温度的关系如下表:
温度/K | 398 | 498 | … |
平衡常数(K) | K1 | K2 | … |
K1 K2(填“>”或“<”),请分析,298K时,合成氨反应能否自发进行 。
(3) 向氨合成塔中充入10molN2和40mol H2进行氨的合成,一定温度(T)下平衡混合物中氨气的体积分数与压强(p)的关系如图1所示。下列说法正确的是 (填字母)。

A.由图可知增大体系压强(p),有利于增大氨气在混合气体中的体积分数
B.若图中T=500℃,则温度为450℃时对应的曲线是b
C.工业上采用500℃温度可有效提高氮气的转化率
D.当3v正(H2)=2v逆(NH3)时,反应达到平衡状态
当温度为T、氨气的体积分数为25%时,N2的转化率为 。
(4)工业上用NH3生产硝酸时,将NH3和O2按体积比1:2混合通入某特定条件的密闭容器中进行反应,所有物质不与外界交换,最后所得溶液中溶质的质量分数为 。
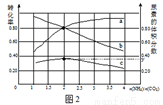
(5)氨碳比[n(NH3)/n(CO2)]对合成尿素的反应:2NH3(g)+CO2(g) CO(NH2)2(g)+H2O(g)有影响。T℃时,在一定体积为2L的恒容密闭容器中,将物质的量之和为3 mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示,a、b分别表示CO2或NH3的转化率,c表示平衡体系中尿素的体积分数。[n(NH3)/n(CO2)] 时,尿素产量最大;该条件下反应的平衡常数K= 。
CO(NH2)2(g)+H2O(g)有影响。T℃时,在一定体积为2L的恒容密闭容器中,将物质的量之和为3 mol的NH3和CO2以不同的氨碳比进行反应,结果如图2所示,a、b分别表示CO2或NH3的转化率,c表示平衡体系中尿素的体积分数。[n(NH3)/n(CO2)] 时,尿素产量最大;该条件下反应的平衡常数K= 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com