
科目:高中化学 来源:2016届重庆市高三上学期第三次月考理综化学试卷(解析版) 题型:选择题
关于下列图示的说法中正确的是:
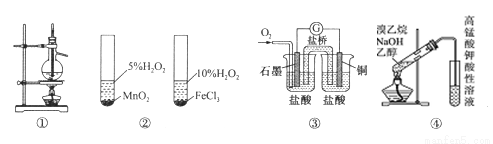
A.图①装置用于分离沸点相关较大的互溶液体混合物
B.图②装置用于研究不同催化剂对反应速率的影响
C.图③中电流计的指针发生偏转,石墨为正极
D.图④装置可用于检验溴乙烷与NaOH的醇溶液共热产生的乙烯
查看答案和解析>>
科目:高中化学 来源:2015-2016学年甘肃省高二上期中(理)化学试卷(解析版) 题型:选择题
对可逆反应4NH3(g) + 5O2(g) 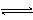 4NO(g) + 6H2O(g),下列叙述正确的是( )
4NO(g) + 6H2O(g),下列叙述正确的是( )
A.达到化学平衡时,若增加容器体积,则正反应速率减小,逆反应速率增大
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态
C.达到化学平衡时,4v正(O2) = 5v逆(NO)
D.化学反应速率关系是:2v正(NH3) = 3v正(H2O)
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南省高二上12月段考化学试卷(解析版) 题型:选择题
反应N2O4(g) 2NO2(g) △H=+57kJ/mol,在温度T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
2NO2(g) △H=+57kJ/mol,在温度T1、T2时,平衡体系中NO2的体积分数随压强变化的曲线如图所示。下列说法正确的是
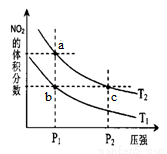
A.a、c两点的反应速率:a>c
B.a、c两点气体的颜色:a浅,c深
C.a、b两点气体的平均相对分子质量:a>b
D. b、c两点化学平衡常数:b<c
查看答案和解析>>
科目:高中化学 来源:2015-2016学年海南省高一上12月段考化学试卷(解析版) 题型:填空题
(1)在Cu+2H2SO4(浓)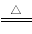 CuSO4+SO2↑+2H2O反应中,请用双线桥法标出元素化合价的升降、电子得失和被氧化、被还原的情况。
CuSO4+SO2↑+2H2O反应中,请用双线桥法标出元素化合价的升降、电子得失和被氧化、被还原的情况。
(2)维生素C能使食物中的Fe3+转化为Fe2+,即Fe3+ Fe2+
Fe2+
①在此变化中,Fe3+被_______(填氧化或还原,下同);维生素C是_______剂
②若有1molFe3+转化为Fe2+,则维生素C______(填得或失)_______mol电子
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:填空题
过渡元素在生活、生产和科技等方面有广泛的用途。
(1)过渡金属离子与水分子形成的配合物是否有颜色,与其d轨道电子排布有关。一般而言,为d0或d10排布时,无颜色;为d1~d9排布时,有颜色,如[Co(H2O)6]2+显粉红色,据此判断,[Mn(H2O)6]2+________(填“有”或“无”)颜色。
(2)现代污水处理工艺中常利用聚合铁{简称PFS,化学式为:[Fe2(OH)n(SO4)3-n/2]m,n<5,m<10}在水体中形成絮状物,以吸附重金属离子。下列说法中不正确的是________。(填序号)
A.PFS中铁显+3价
B.铁原子的外围电子排布式是3d64s2
C.由FeSO4溶液制PFS需经过氧化、水解和聚合的过程
D.由下表可知气态Fe2+再失去一个电子比气态Mn2+再失去一个电子难
元素 | Mn | Fe | |
电离能 | I1 | 717 | 759 |
(kJ·mol-1)[ | I2 | 1 509 | 1 561 |
I3 | 3 248 | 2 957 | |
(3)铬的配合物在药物应用、设计合成新磁材料领域和聚乙烯催化剂方面都有重要应用。现有铬(Ⅲ)与甲基丙烯酸根的配合物为: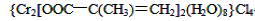
①该化合物中存在的化学键类型有______________________________。
②甲基丙烯酸分子中C原子的杂化方式有________。
③等电子体是具有相同的价电子数和原子数的分子或离子,与H2O分子互为等电子体的微粒是________(填一种即可)。
④与铬同周期的所有元素中基态原子最外层电子数与铬原子相同的元素是________(填元素符号)。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二上12月月考化学试卷(解析版) 题型:选择题
在半导体生产或灭火剂的使用中,会向空气逸出气体如:NF3、CHClFCF3、C3F8,它们虽是微量的,有些确是强温室气体。下列推测不正确的是 ( )
A.由价层电子对互斥理论可确定NF3分子呈三角锥型
B.C3F8在CCl4中的溶解度比水中大
C.CHClFCF3存在手性异构
D.第一电离能:N<O<F
查看答案和解析>>
科目:高中化学 来源:2015-2016学年内蒙古赤峰二中高一上第二次月考化学试卷(解析版) 题型:填空题
(1)赤铜矿的主要成分是Cu2O,辉铜矿的主要成分是Cu2S。赤铜矿与辉铜矿混合加热发生以下反应:Cu2S+2Cu2O===6Cu+SO2。氧化剂是________,还原剂是________每生成19.2 g Cu,反应中转移电子数_________
(2)已知8NH3+3Cl2 = 6NH4Cl+N2,氧化剂与还原剂的分子个数比为________;当有4mol NH3被氧化时,生成的还原产物为________ g。
查看答案和解析>>
科目:高中化学 来源:2016届福建省高三上12月月考化学试卷(解析版) 题型:选择题
用CO合成甲醇的反应为:CO(g)+2H2(g)═CH3OH (g)△H<0.按照相同的物质的量投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示.下列说法正确的是( )

A.温度:T1>T2>T3
B.正反应速率:v(a)>v(c) v(b)>v(d)
C.平衡常数:K(a)>K(b) K(b)=K(d)
D.平均摩尔质量: M(a)>M(c) M(b)<M(d)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com