
【题目】25℃时,将 1.0 L ![]() moI/L CH3COOH 溶液与 0.1 mol NaOH固体混合,充分反应后向混合液中加入CH3COOH或CH3COONa固体(忽略前后体积和温度变化),引起溶液pH的变化如图所示。 下列叙述正确的是
moI/L CH3COOH 溶液与 0.1 mol NaOH固体混合,充分反应后向混合液中加入CH3COOH或CH3COONa固体(忽略前后体积和温度变化),引起溶液pH的变化如图所示。 下列叙述正确的是
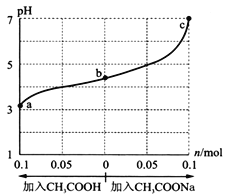
A. b点混合液中存在c(Na+)=c(CH3COO-)+c(CH3COOH)
B. a、b、c三点对应的混合液中,水的电离程度由大到小的顺序是 c<b<a
C. 在加入CH3COOH的过程中,![]() 减小
减小
D. 由图可知,常温下CH3COOH的电离平衡常数Ka= ![]() mol/L
mol/L
【答案】C
【解析】1.0L xmolL-1 CH3COOH溶液与0.1mol NaOH固体混合,混合后溶液的pH<5,显酸性,说明醋酸过量,溶液中溶质为CH3COOH和CH3COONa;加醋酸时,酸的量增多,使溶液酸性增强;加CH3COONa时,CH3COONa本身水解显碱性,相当于加碱,使溶液酸性减弱,最终达到中性。A.b点溶液pH<5,溶液显酸性,溶液中c(H+)>c(OH-),溶液中存在电荷守恒,c(Na+)+c(H+)=c(OH-)+c(CH3COO-),由于c(H+)>c(OH-),所以c(Na+)<c(CH3COO-),故A错误;B.溶液中酸或碱电离的氢离子或氢氧根离子的浓度越大,水的电离程度越小,a、b、c三点溶液中氢离子浓度依次减小,水的电离程度增大,所以水的电离程度由大到小的顺序的是c>b>a,故B错误;C.向混合液中加入CH3COOH固体,忽略溶液体积的变化,则溶液中c(Na+)不变,溶液中![]() =
=![]() ,因此溶液中
,因此溶液中![]() =
=![]() ,随着CH3COOH固体的不断加入,溶液中c(CH3COOH)不断增大,则该值减小,故C正确;D.pH=7时,溶液中c(H+)=c(OH-),溶液中存在电荷守恒,则c(Na+)+c(H+)=c(OH-)+c(CH3COO-),由于c(H+)=c(OH-),则此时溶液中c(Na+)=c(CH3COO-),根据图象,c(H+)=10-7molL-1,c(Na+)=c(CH3COO-)=0.2mol/L,则醋酸的电离平衡常数为Ka=
,随着CH3COOH固体的不断加入,溶液中c(CH3COOH)不断增大,则该值减小,故C正确;D.pH=7时,溶液中c(H+)=c(OH-),溶液中存在电荷守恒,则c(Na+)+c(H+)=c(OH-)+c(CH3COO-),由于c(H+)=c(OH-),则此时溶液中c(Na+)=c(CH3COO-),根据图象,c(H+)=10-7molL-1,c(Na+)=c(CH3COO-)=0.2mol/L,则醋酸的电离平衡常数为Ka=![]() =
=![]() mol/L,故D错误;故选C。
mol/L,故D错误;故选C。


 黄冈课堂作业本系列答案
黄冈课堂作业本系列答案 单元加期末复习先锋大考卷系列答案
单元加期末复习先锋大考卷系列答案科目:高中化学 来源: 题型:
【题目】下列表述正确的是:
A. 某离子M层上和L层上的电子数均为K层的4倍
B. Cl-的结构示意图: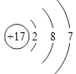
C. 某物质的焰色反应为黄色,某物质一定为钠的化合物
D. 14C和14N的质量数相等,互称为同位素
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】离子的摩尔电导率可用来衡量电解质溶液中离子导电能力的强弱,摩尔电导率越大,离子在溶液中的导电能力越强。已知Ca2+、OH-、HCO3—的摩尔电导率分别为0.60、1.98、0.45,据此可判断,向饱和的澄清石灰水中通入过量的二氧化碳,溶液导电能力随二氧化碳通入量的变化趋势正确的是( )
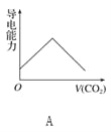
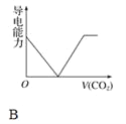

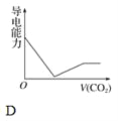
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮氧化合物是目前造成大气污染的主要气体,而汽车尾气中就含有NO 等多种污染气体。汽车尾气里含有的NO气体是由于内燃机燃烧的高温引起氮气和氧气反应所致。请结合所学知识回答下列问题:
(1) 已知:N2(g)+2O2(g)![]() 2NO2(g) △H1=+67.8 kJ/mol
2NO2(g) △H1=+67.8 kJ/mol
2NO2(g)![]() O2(g)+2NO(g) △H2=+116.2 kJ/mol
O2(g)+2NO(g) △H2=+116.2 kJ/mol
则N2(g)+O2(g)![]() 2NO(g) △H=_________kJ/mol;汽车启动后,气缸温度越高,单位时间内NO 的排放量越大,分析其原因为_____________
2NO(g) △H=_________kJ/mol;汽车启动后,气缸温度越高,单位时间内NO 的排放量越大,分析其原因为_____________
(2) 若反应N2(g)+O2(g)![]() 2NO(g)是在恒容条件下进行,下列能说明该反应已达到平衡状态的是________
2NO(g)是在恒容条件下进行,下列能说明该反应已达到平衡状态的是________
a.2υ正(N2)= υ逆(NO) b.混合气体密度不变
c.生成1molO2的同时生成2molNO d.混合气体平均相对分子质量不变
(3) 汽车尾气净化反应:2NO(g)+2CO(g)![]() N2(g)+2CO2(g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:
N2(g)+2CO2(g) △H= -746.5 kJ/mol,若将0.20molNO和0.10molCO充入一个容积恒定为1L 的密闭容器中,在不同条件下,反应过程中部分物质的浓度变化状况如图所示:
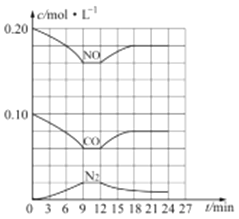
①该反应能自发进行的条件为_____ (填“高温”、“低温”或“任意温度”);
②在6~9 min 内,以CO 表示的平均反应速率 υ(CO)=________mol·L-l·min-1;
③第12min时改变的反应条件为_________ (填“升高温度”或“降低温度”);
④反应在第24min时的平衡常数K=____________(只列出计算式,无需计算结果),若保持温度不变,再向容器中充入CO、N2 各0.060mol,平衡将_________移动(填“正向”、“逆向”或“不”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】关于下列装置说法正确的是
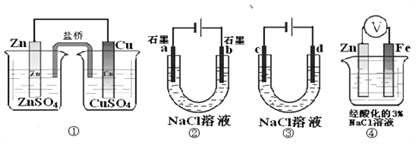
A. 装置①中,盐桥中的Cl-移向CuSO4溶液
B. 装置②工作一段时间后,a极表面生成了较多的O2
C. 用装置③精炼铜时,c极为粗铜
D. 装置④中电子由Zn流向Fe,Zn极发生氧化反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】北魏贾思勰《齐民要术·作酢法》这样描述苦酒:“乌梅苦酒法:乌梅去核,一升许肉,以五升苦酒渍数日,曝干,捣作屑。欲食,辄投水中,即成醋尔。”下列有关苦酒主要成分的说法正确的是( )
A. 苦酒的主要溶质是非电解质 B. 苦酒的主要溶质是弱电解质
C. 苦酒的主要溶质是强电解质 D. 苦酒的溶液中只存在分子,不存在离子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】过氧乙酸(![]() )是一种高效消毒剂,常用于环境消毒杀菌,可以迅速杀死多种微生物。它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:
)是一种高效消毒剂,常用于环境消毒杀菌,可以迅速杀死多种微生物。它可由冰醋酸和过氧化氢在浓硫酸催化作用下制得,实验装置和步骤如下:
①在三颈烧瓶中加入一定量冰醋酸与浓H2SO4的混合液体,再缓缓加入适量30%的双氧水。
②不断搅拌并控制B中混合液的温度为20~30℃至反应结束。
③接入冷凝管和抽气泵,在锥形瓶中收集得到产品。
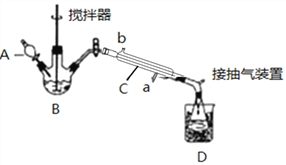
请回答下列问题:
(1)仪器C的名称是_______________;仪器C中冷水流入口是_____(填a或b);
(2)为更好地控制反应温度,应采用方法是_________________;
(3)生成过氧乙酸的化学方程式为________________________________________;
(4)不同反应物比例,实验测得生成过氧乙酸含量(%)随时间的变化数据(见下表),由表中数据可知,反应物最佳比例(CH3COOH/H2O2)是______,反应所需时间约________(选填1、3、5、7)小时;
反应物比例CH3COOH/H2O2 | 反应时间(小时) | ||||
0.5 | 1 | 3 | 5 | 7 | |
2:1 | 7.38 | 8.46 | 9.42 | 11.26 | 13.48 |
1:1 | 10.56 | 12.92 | 13.54 | 20.72 | 20.70 |
1:2 | 6.14 | 7.10 | 7.96 | 10.38 | 12.36 |
(5)请设计实验比较Fe3+、Cu2+对过氧乙酸的催化效率;可供选择的试剂和主要器材有:a.过氧乙酸溶液、b.1mol/L的FeCl3溶液、c.0.5mol/L的Fe2(SO4)3溶液、d.0.5mol/L的CuCl2溶液、e.1mol/L的CuSO4溶液、f.计时器、g.测量气体体积的针筒、i.带导气管的试管。
你选择的试剂及器材是a、_______、f、g、i(选填序号),实验方案是_________________________。
(6)碘量法分析:取2.00mL过氧乙酸试样稀释成
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关硅及其化合物的叙述中,错误的是
A.单质硅是良好的半导体材料
B.硅和碳是都是第ⅣA族的元素
C.二氧化硅用来制造通讯材料(光导纤维)
D.二氧化硅溶于水生成硅酸,它是挥发性酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图为元素在生物体内的含量分布情况,下列表述不正确的是( )
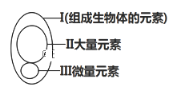
A. Ⅰ在非生物界中都能找到,体现了生物界与非生物界的统一性
B. Ⅲ含量虽少,却是生物体正常生命活动不可缺少的
C. Ⅱ和Ⅲ为生物体的必需元素,一旦缺乏就可能会导致相应的病症
D. P、S、K、Ca、Zn属于大量元素
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com