
 Q��W��X��Y��Z��5�ֶ�����Ԫ�أ�ԭ������������Q�����ڱ��а뾶��С��Ԫ�أ�W��Y��ɵĻ��������������塢X��Y��ɵĻ������ǻ������ų��Ĵ�����Ⱦ�Y��Z���γ�ԭ�Ӹ�����Ϊ1��1��1��2���������ӻ����
Q��W��X��Y��Z��5�ֶ�����Ԫ�أ�ԭ������������Q�����ڱ��а뾶��С��Ԫ�أ�W��Y��ɵĻ��������������塢X��Y��ɵĻ������ǻ������ų��Ĵ�����Ⱦ�Y��Z���γ�ԭ�Ӹ�����Ϊ1��1��1��2���������ӻ���� ��
������ Q��W��X��Y��Z��5�ֶ�����Ԫ�أ�ԭ������������Y��Z���γ�ԭ�Ӹ�����Ϊ1��1��1��2���������ӻ������Y��OԪ�ء�Z��NaԪ�أ�
Q��W��ɵĻ�������һ���������壬Q��ԭ������С��W���������Ǽ��飬��Q��HԪ�ء�W��CԪ�أ�
W��Y��X��Y��ɵĻ������ǻ������ų��Ĵ�����Ⱦ���X��ԭ����������W��С��Y������X��NԪ�أ��ٽ��ԭ�ӽṹ����ѧƽ�⡢ԭ���ԭ�����
��� �⣺Q��W��X��Y��Z��5�ֶ�����Ԫ�أ�ԭ������������Y��Z���γ�ԭ�Ӹ�����Ϊ1��1��1��2���������ӻ������Y��OԪ�ء�Z��NaԪ�أ�Q��W��ɵĻ�������һ���������壬Q��ԭ������С��W���������Ǽ��飬��Q��HԪ�ء�W��CԪ�أ�W��Y��X��Y��ɵĻ������ǻ������ų��Ĵ�����Ⱦ���X��ԭ����������W��С��Y������X��NԪ�أ�
��1��YΪOԪ�أ��ڶ����ڵڢ�A��Ԫ�أ�X�γɵĵ����ǵ��������������д��ڵ�����������ԭ�������Ϊ8���ӣ���N2�ĵ���ʽΪ ��
��
�ʴ�Ϊ���ڶ����ڵڢ�A�壻 ��
��
��2��Q2ΪH2��Y2ΪO2��H2��O2�ķ�Ӧ�ɽ���ѧ��ת��Ϊ���ܣ����ݵ�������֪��a�Ǹ�����b��������a�缫��ͨ��H2��H2ʧ���Ӻ����������ӷ�Ӧ����ˮ���缫��ӦʽΪ��H2+2OH--2e-=2H2O��
�ʴ�Ϊ��H2+2OH--2e-=2H2O��
��3��X��Z��ɵ�һ�����ӻ��������ˮ��Ӧ�������ּ���������Na3N��Na3N��ˮ��Ӧ�����������ƺ�һˮ�ϰ������Ը÷�Ӧ�Ļ�ѧ����ʽΪ��Na3N+4H2O=3NaOH+NH3•H2O���ʴ�Ϊ��Na3N+4H2O=3NaOH+NH3•H2O��
���� ���⿼����λ�ýṹ���ʵ����ϵ��Ӧ�ã���Ŀ�Ѷ��еȣ������ƶϸ�Ԫ��Ϊ���ؼ���ע����ȷԭ���ԭ������Ӧ�ã���������ԭ�ӽṹ��Ԫ�����ڱ���Ԫ�������ɵĹ�ϵ��


 ȫ��������ϵ�д�
ȫ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
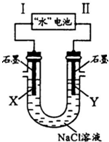 �о���Ա������һ�֡�ˮ����أ����ܷ�ӦΪ��5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl����ͼ�á�ˮ�����Ϊ��Դ���NaCl��Һ��ʵ���У�X�缫������ɫ�����ݳ��������йط�����ȷ���ǣ�������
�о���Ա������һ�֡�ˮ����أ����ܷ�ӦΪ��5MnO2+2Ag+2NaCl=Na2Mn5O10+2AgCl����ͼ�á�ˮ�����Ϊ��Դ���NaCl��Һ��ʵ���У�X�缫������ɫ�����ݳ��������йط�����ȷ���ǣ�������| A�� | IΪ��������缫��ӦʽΪAg+Cl-+e-=AgCl | |
| B�� | ��ˮ�������Na+�������������ƶ� | |
| C�� | ÿת��1 mol e-��U��������0.5 mol H2O | |
| D�� | ��ˮ������ڣ�ÿ����1 mol Na2Mn5O10��X�缫������1 mol���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | NH2-CH2-COOH | |
| B�� | NH2-CH2-CH2OH | |
| C�� |  | |
| D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ���� | �����Լ� | ʵ������ |
| �� | 2�� 0.1mol/L��FeCl3����Һ | �ٰ�ɫ����ת��Ϊ���ɫ���� |
| �� | 4mL2mol/LNH4Cl��Һ | �ڰ�ɫ�����ܽ⣬����ɫ��Һ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ϡ�����������м��Ӧ��Fe+4H++NO3-�TFe3++NO��+2H2O | |
| B�� | ̼������Һˮ������ӷ���ʽ��CO32-+2H2O?H2CO3+2OH- | |
| C�� | ������ȼ����Ϊ285.8 kJ/mol�����ʾ����ȼ�յ��Ȼ�ѧ����ʽΪ��2H2��g��+O2��g���T2H2O��g����H=-571.6 kJ/mol | |
| D�� | Ũ������MnO2������������MnO2+4H++2Cl-$\frac{\underline{\;\;��\;\;}}{\;}$Mn2++Cl2��+2H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH3CH2OH+CH3COOH��$?_{��}^{Ũ����}$CH3COOCH2CH3+H2O | |
| B�� | CH3CH2OH$��_{170��}^{Ũ����}$CH2=CH2��+H2O | |
| C�� | 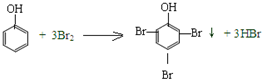 | |
| D�� | CH3CH2OH+HBr$\stackrel{��}{��}$CH3CH2Br+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ϡ���������ɫ���壬������ͨ�����ʯ��ˮ�У���Һ����ǣ�һ����CO32- | |
| B�� | ij��������ɫ��Ӧʱ������ʻ�ɫ����������п϶������ڼ�Ԫ�� | |
| C�� | ��������������Һ�����ȣ�������������ʹʪ���ɫʯ����ֽ������һ����NH4+ | |
| D�� | �����Ȼ�����Һ�а�ɫ�����������ټ����ᣬ��������ʧ��һ����SO42- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
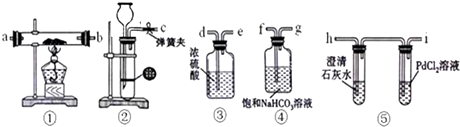
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com