
| |||||||||||||||||||
(1) |
Na2O |
(2) |
2Na2O2+2H2O |
(3) |
负极,Cl2+2e- |
(4) |
答案:Cu+H2O2+2H+ 精析:符合A2B2类型的化合物常见的有H2O2、Na2O2,根据X2Y2是共价化合物,Z2Y2是离子化合物,确定X为H元素、Y为O元素、Z为Na元素.XW、ZW中W元素为-1价,可知W为ⅦA族元素,它的原子序数比Na大,且处于短周期,确定W为Cl元素. 接通S1时,图示装置为电解池.其中阴极反应:2H2O+2e- 断开S1,接通S2,电流表的指针发生偏转,说明图示装置为原电池,各电极上发生的反应与之前正好相反,C(Ⅰ):2OH-+H2-2e- |


科目:高中化学 来源: 题型:
![]() X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无气味的气体。这四种化合物具有如下图的转化关系(部分反应物、产物及反应条件已略去)。
X、Y、Z、W四种化合物均由短周期元素组成,其中X含有四种元素,X、Y、Z的焰色反应均为黄色,W为无色无气味的气体。这四种化合物具有如下图的转化关系(部分反应物、产物及反应条件已略去)。
![]()
![]()
![]()
![]() 请回答:
请回答:
![]() (1)W为 分子(填“极性”或“非极性”)。
(1)W为 分子(填“极性”或“非极性”)。
![]() (2)X与Y在溶液中反应的离子方程式是 。
(2)X与Y在溶液中反应的离子方程式是 。
![]() (3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体。
(3)X含有的四种元素之间(二种、三种或四种)可组成多种化合物,选用其中某些化合物,利用下图装置(夹持固定装置已略去)进行实验,装置Ⅲ中产生白色沉淀,装置Ⅴ中可收集到一种无色气体。
![]()
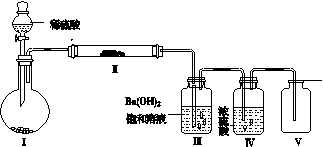
![]() ①装置Ⅰ中反应的化学方程式是: ,
①装置Ⅰ中反应的化学方程式是: ,
![]() 装置Ⅱ中物质的电子式是: 。
装置Ⅱ中物质的电子式是: 。
![]() ②用X含有的四种元素中的两种组成的某化合物M,在催化剂存在的条件下制备并收集纯净干燥的装置Ⅴ中的气体,该化合物M的结构式是 ,所需仪器装置是 (从上图中选择必要装置,填写编号)。
②用X含有的四种元素中的两种组成的某化合物M,在催化剂存在的条件下制备并收集纯净干燥的装置Ⅴ中的气体,该化合物M的结构式是 ,所需仪器装置是 (从上图中选择必要装置,填写编号)。
![]() (4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是 。
(4)向Z溶液中通入氯气,可制得某种生产和生活中常用的漂白、消毒的物质,同时有X生成,该反应的化学方程式是 。
查看答案和解析>>
科目:高中化学 来源: 题型:
T、X、Y、Z、R、W为周期表前四周期元素,原子序数依次递增。已知:
①W原子最外层有1个电子,属于ds区元素,其余的均为短周期主族元素;
②T原子所处的周期数、族序数分别与其原子序数相等;
③X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同;
④Z的基态原子价电子排布为ns2npn+2;
⑤R的单质常温常压下是气体,其基态原子的M层上有1个未成对的p电子;
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是 __________ ___(用元素符号表示)。
(2)Y的氢化物分子间能形成氢键,R的氢化物分子间不易形成氢键,原因是 。
(3)W的基态原子的价层电子排布式为 ,该元素与元素Y 、T能形成的[W(YT3)4]2+离子中,含有的化学键是 。
a.离子键 b.极性键 c.非极性键 d.配位键
画出其结构式_____________
(4) T、X、Z三种元素组成的一种化合物M是新装修居室中常见的有害气体,它的分子式为XT2Z,分子空间构型为平面三角形,则该分子中中心原子采取_____ 杂化,1molM分子中σ键和π键的个数比为 。
(5) T和Z可以形成个数比为1:1的分子,其中中心原子采取 杂化;通常情况下,该分子与水任意比互溶的主要原因是 。
查看答案和解析>>
科目:高中化学 来源:2012届辽宁省锦州中学高三第一次月考化学试卷 题型:填空题
T、X、Y、Z、R、W为周期表前四周期元素,原子序数依次递增。已知:
①W原子最外层有1个电子,属于ds区元素,其余的均为短周期主族元素;
②T原子所处的周期数、族序数分别与其原子序数相等;
③X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同;
④Z的基态原子价电子排布为ns2npn+2;
⑤R的单质常温常压下是气体,其基态原子的M层上有1个未成对的p电子;
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是 __________ ___(用元素符号表示)。
(2)Y的氢化物分子间能形成氢键,R的氢化物分子间不易形成氢键,原因是 。
(3)W的基态原子的价层电子排布式为 ,该元素与元素Y 、T能形成的[W(YT3)4]2+离子中,含有的化学键是 。
a.离子键 b.极性键 c.非极性键 d.配位键
画出其结构式_____________
(4) T、X、Z三种元素组成的一种化合物M是新装修居室中常见的有害气体,它的分子式为XT2Z,分子空间构型为平面三角形,则该分子中中心原子采取_____ 杂化,1molM分子中σ键和π键的个数比为 。
(5) T和Z可以形成个数比为1:1的分子,其中中心原子采取 杂化;通常情况下,该分子与水任意比互溶的主要原因是 。
查看答案和解析>>
科目:高中化学 来源:2011-2012学年辽宁省高三第一次月考化学试卷 题型:填空题
T、X、Y、Z、R、W为周期表前四周期元素,原子序数依次递增。已知:
①W原子最外层有1个电子,属于ds区元素,其余的均为短周期主族元素;
②T原子所处的周期数、族序数分别与其原子序数相等;
③X的基态原子中电子占据三种能量不同的原子轨道,且每种轨道中的电子数相同;
④Z的基态原子价电子排布为ns2npn+2;
⑤R的单质常温常压下是气体,其基态原子的M层上有1个未成对的p电子;
(1)X、Y、Z三种元素的第一电离能由大到小的顺序是 __________ ___(用元素符号表示)。
(2)Y的氢化物分子间能形成氢键,R的氢化物分子间不易形成氢键,原因是 。
(3)W的基态原子的价层电子排布式为 ,该元素与元素Y 、T能形成的[W(YT3)4]2+离子中,含有的化学键是 。
a.离子键 b.极性键 c.非极性键 d.配位键
画出其结构式_____________
(4) T、X、Z三种元素组成的一种化合物M是新装修居室中常见的有害气体,它的分子式为XT2Z,分子空间构型为平面三角形,则该分子中中心原子采取_____ 杂化,1molM分子中σ键和π键的个数比为 。
(5) T和Z可以形成个数比为1:1的分子,其中中心原子采取 杂化;通常情况下,该分子与水任意比互溶的主要原因是 。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com