
������Ʒ�������п�����������������Ʒ�ı�������һ�����ܵ�Fe3O4��ijѧϰС��Ϊ���о�������Ƭ���ֱ����������ʵ�������
�ٰ�һ����������Ƭ�ӹ��ɾ��ȷ�ĩ��
��ȡm g�÷�ĩ������28.00 mL 1 mol��L�������У�ǡ����ȫ��Ӧ�����ɱ�״���µ�����134.4 mL������Һ�е���KSCN��Һ������������
����ȡ���ݲ�ͬ�����ķ�ĩ���ּӼӵ���ͬ���(V)�����ʵ���Ũ�Ⱦ�Ϊl0.00 mol��L������������Һ�У���ַ�Ӧ����ȫ���ܽ⣬�йص�ʵ���������±���ʾ(����NO�������Ψһ��ԭ����)��
| ʵ����� | �� | �� | �� |
| �����ĩ����/g | 13.68 | 27.36 | 34.20 |
| ����������������״����/L | 2.912 | 5.824 | 6.720 |
��1��FeCl2��4��1 �� 0.912 g
��2��180 mL
��3��0.105mol��n(Cu)��0.315mol
���������������1����������Һ�е���KSCN��Һ�������������֪��Ӧ�����ɵ�����ΪFeCl2�����ڷ����������Ϊ28.00 mL�� 1 mol��L=0.028mol���ʲ���FeCl2�����ʵ���Ϊ0.028/2=0.014mol�����е������ֱ������ᡢFe3O4���߷�����Ӧ���������ɱ�״���µ�����134.4 mL�����ݵ���غ��֪��������������ᷢ����������ĵ�����Ϊ0.006mol����Fe3O4��Fe��HCl��ͬ��Ӧ���ڸ÷�Ӧ����Ԫ������Ϊ��0.014mol-0.006mol=0.008mol���Ҹ÷�Ӧ����ʽΪFe3O4+8HCl+Fe=4FeCl2+4H2O��ͨ���÷�Ӧ����ʽ��֪Fe3O4Ϊ0.002mol�������÷�Ӧ�ĵ�����Ϊ0.002mol�����ܵ�Fe���ʵ���Ϊ0.008mol��Fe3O4Ϊ0.002mol���ʱ���Ϊ4��1������Ϊ0.002mol��232g/mol +0.008mol��56g/mol =0.912g��
��2����������ʵ�飬ͨ��Ͷ���ĩ�����������������������ϵ��֪����Ϊ�����������Ϊ��ĩ��������ͨ��ʵ��������������������ڼ���NO�������Ψһ��ԭ����Ҳ�������������ʵ���Ϊ6.720L/22.4L��mol-1=0.3mol����NԪ�صõ�������Ϊ0.3mol��3=0.9mol�����ڢ��л��������Ϊ34.2g����n(Fe)��n(Fe3O4)=4:1����FeΪ0.3mol��Fe3O4Ϊ0.075mol�����ڵ�Ԫ�صõ���������Ϊ0.9mol������Һ��ΪFe(NO3)2��Fe(NO3)3�������ʣ������֪Fe(NO3)2Ϊ0.075mol��Fe(NO3)3Ϊ0.45mol������Һ�����������Ϊ0.075mol��2+0.45mol��3=1.5mol����÷�Ӧ��NԪ�������ʵ���Ϊ1.5mol+0.3mol=1.8mol������������Ϊ180ml��
��3��27.36g ��ĩ������n(Fe)��n(Fe3O4)=4:1��֪����Ԫ��0.42mol�������������������Ϊ����������II��Ӧ��������1.52 mol(���Ṳ1.8mol)����II��Һ����Fe3+ 0.42 mol����������0.28mol��
3Cu ~ 8HNO3 Cu ~ 2Fe3+
3 8 1 2
nmin 0.28mol n 0.42
nmin=0.105mol n=0.21mol nmax =0.21mol+0.105mol=0.315mol
���㣺��ѧ���㡢�����غ㣬�����غ㡢��ѧ����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
��ҵ�Ʊ��Ȼ�ͭʱ����Ũ����������������80 �����ң����������CuO��ĩ(������Fe2O3��FeO)����ֽ��裬ʹ֮�ܽ⣬��һǿ���ԵĻ����Һ�������Ӹû����Һ���Ʊ�������CuCl2��Һ���������²���[�ο����ݣ�pH��9.6ʱ��Fe2����ȫˮ���Fe(OH)2��pH��6.4ʱ��Cu2����ȫˮ���Cu(OH)2��pH��3.7ʱ��Fe3����ȫˮ���Fe(OH)3]����ش��������⣺
��1����һ����ȥFe2�����ܷ�ֱ�ӵ�����ҺpH��9.6����Fe2��������ȥ�� ������ܡ� ���ܡ��������� ��
��2��������ǿ������NaClO�Ƚ�Fe2������ΪFe3�����ٵ�����Һ��PH��Fe3��������ȥ��
�ټ���NaClO����Һ��pH�仯��________(�����)��
A��һ������ B��һ����С C���������� D�����ܼ�С
������Ϊ��NaClO���������Ƿ����� ������ǡ� ���������м��ֳ��õ��������������ڳ�ȥ�����Һ��Fe2������________(�м���ѡ�����������)��
A��ŨHNO3 B��Cl2 C��KMnO4 D��H2O2
��3�������ʵ����ʵ�����ҺpH��ʹFe3+ת��ΪFe(OH)3���������Դﵽ��ȥFe3+������ʧCuCl2��Ŀ�ģ��������ҺpH��ѡ�����������е�___________��
A��NaOH B��NH3��H2O C��CuO D��Cu(OH)2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ʴ���
��15�֣�
��������ͭ�Ƚ������仯�������ճ�������Ӧ�ù㷺�����������ʵ��ش����⣺
��1������������ ���壬��FeCl3��Һ�������ɡ��������õ������� ���ѧʽ����
��2����д����������������Һ��Ӧ�Ļ�ѧ����ʽ____
��3������Cu�����백ˮ����˫��ˮ������Ӧ����������ߵĻ����Һ��Ӧ��������ɫ��Һ��������ɫ��Ũ��Һ�м����Ҵ��������������� ������������ɫ�����ӵĽṹʽ____ д��Cu�백ˮ��˫��ˮ��Ӧ�����ӷ���ʽ��____
��4��������������Һ�м��������̼����泥���FeCO3�������ɣ�д���仯ѧ����ʽ____
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�̷�(FeSO4��7H2O)���ᷨ����һ��ϡ�н�����Ʒ�����в����ĸ���Ʒ����Ʒ���Ϊ����ɫ����ɫ�ᾧ���塣���������ɵ��ڼ���ˮ�е�pH����ˮ���������л���ϣ������ٳ�������ҪӦ����ˮ�ʾ�����ҵ��ˮ������ͬʱ����ɱ�����á�
��1��98% 1.84 g/cm3��Ũ������ϡ�����У��ܶ��½�����ϡ����50%ʱ���ܶ�Ϊ1.4g/cm3��50%���������ʵ���Ũ��Ϊ (������λС��)��50%��������30%������������ϣ�������Ũ��Ϊ (��>��<��=")40%" ��
��2��ʵ��������20%��������(100�˷������ẬSO3 20��)����ϡ���ᣬ����SO3��nH2O��ʾ20%�ķ������ᣬ��n=____________(������λС��)��
��3���̷��ڿ��������ױ���������Ϊ����������ȡ7.32�˾�������ϡ�������������BaCl2��Һ�����˵ó���9.32�ˣ���ͨ��112mL(��״��)����ǡ�ý�Fe2����ȫ�������Ʋ⾧��Ļ�ѧʽΪ ��
��4����������泥�(NH4)2SO4��FeSO4��6H2O��(�׳�Ī����)�����̷��ȶ����ڷ�����ѧ�г���������Fe2+�ı���Һ���ô�Fe2+�ı���Һ���Բⶨʣ��ϡ�����������ȡ8.64��Cu2S��CuS�Ļ������200 mL 2 mol/Lϡ������Һ������������Ӧ���£�
10NO3-��3Cu2S��16H��=6Cu2����10NO����3SO42-��8H2O
8NO3-��3CuS��8H��=3Cu2����3 SO42-��8NO��+ 4H2O
ʣ���ϡ����ǡ����V mL 2 mol/L (NH4)2Fe(SO4)2��Һ��ȫ��Ӧ��
��֪��NO3-��3Fe2����4H��= NO����3Fe3+��2H2O
�� Vֵ��Χ ��
�� ��V=48���Լ���������CuS���������� (������λС��)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�������
�Ը������������Ĺ�ҵ��ҺΪԭ�������������Ĺ�������(���ֲ�����������)��
��.�ӷ�Һ���ᴿ���ᾧ��FeSO4��7H2O��
��.��FeSO4��7H2O���Ƴ���Һ��
��.FeSO4��Һ���Թ�����NH4HCO3��Һ��ϣ��õ���FeCO3����Һ��
��.����Һ���ˣ���90 ����ˮϴ�ӳ����������õ�FeCO3���塣
��.����FeCO3���õ�Fe2O3���塣
��֪��NH4HCO3����ˮ�л�ֽ⡣
�Ţ��У�����������м��ȥ��Һ�е�Fe3�����÷�Ӧ�����ӷ���ʽ�� ��
�Ƣ��У����һ�����ᣬ��������� �����û�ѧƽ��ԭ���Լ����ӷ���ʽ������������� ��
�Ǣ��У�����FeCO3�����ӷ���ʽ�� ����FeCO3��Һ��ʱ�䱩¶�ڿ����У����в��ֹ�������Ϊ���ɫ���ñ仯�Ļ�ѧ����ʽ�� ��
(4)���У�ͨ������SO42-���жϳ����Ƿ�ϴ�Ӹɾ�������SO42-�IJ�����
(5)��֪����FeCO3�Ļ�ѧ����ʽ��4FeCO3��O2 =2Fe2O3��4CO2��������464.0 kg��FeCO3���õ�316.8 kg��Ʒ������Ʒ������ֻ��FeO����ò�Ʒ��Fe2O3�������� kg��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
ѧϰС���ijƷ��������Ħ�����ɷּ��京����������̽����
������ϣ� ������Ħ������̼��ơ�����������ɣ������������ɷ���������ʱ���������ɡ�
��Ħ���������������Ķ��Լ��飺 ȡ����������Ʒ����ˮ���衢���ˡ�
��1���������м������NaOH��Һ�����ˡ�����������NaOH��Һ��Ӧ�����ӷ���ʽ��______________��
��2������1��������Һ����ͨ�����������̼���ټ������ϡ���ᡣ�۲쵽��������________________��
��������Ʒ��̼��ƵĶ����ⶨ��������ͼ��ʾװ�ã�ͼ�мг�������ȥ������ʵ�飬��ַ�Ӧ�ⶨC�����ɵ�BaCO3������������ȷ��̼��Ƶ�����������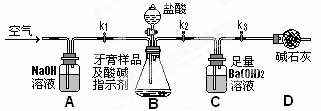
����ʵ����̻ش��������⣺
��3��ʵ����������������ͨ������������ó��˿ɽ���B��C�еķ�Ӧ���⣬����______
��4��C�з�Ӧ����BaCO3�Ļ�ѧ����ʽ��__________________________
��5�����и����ʩ�У�������߲ⶨȷ�ȵ���_________�����ţ���
A���ڼ�������֮ǰ��Ӧ�ž�װ���ڵ�CO2���壻
B���μ�����˹��죻
C����A��B֮������ʢ��Ũ�����ϴ��װ��
D����B��C֮������ʢ�б���̼��������Һ��ϴ��װ��
��6��ʵ����ȷ��ȡ8.00g��Ʒ���ݣ��������βⶨ�����BaCO3ƽ������Ϊ3.94g������Ʒ��̼��Ƶ���������Ϊ_________��
��7��������Ϊ���زⶨC�����ɵ�BaCO3������ֻҪ�ⶨװ��C������CO2ǰ��������һ������ȷ��̼��Ƶ�����������ʵ��֤�����˷����ⶨ�Ľ������ƫ�ߣ�ԭ����______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
(12��)��29����˻����ƻ�����Dz����Ǹ�ǿ�ȵ���þ�Ͻ�ij����С��������þ�Ͻ�����о����ⶨ����þ�����������������������ᡢ����������Һ��������ֲ�ͬ��ʵ�鷽����
����һ����þ�Ͻ� �ⶨ������������
�ⶨ������������
����������þ�Ͻ� �ⶨ������������
�ⶨ������������
����������þ�Ͻ� ��Һ
��Һ �������ղ����������
�������ղ����������
��1��д������һ�з�����Ӧ�����ӷ���ʽ ��
��2��ʵ��С����ݷ��������������ʵ��װ�ã�����Ȧ(ͼ�е�����̨��ʡ��)��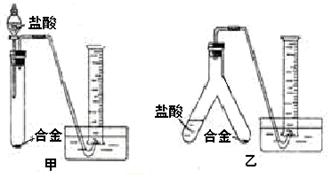
����Ϊѡ�� ��ѡ�����)װ�ý���ʵ�������������С��
��3���÷���������ʵ��ʱ�����˳������ղ��������⣬����������� ��
��4����չ�о���������þ�Ͻ�������������Һ�м������NaOH��Һʱ�����ɳ��������������NaOH��Һ����Ĺ�ϵ���������ϵ��ʾ��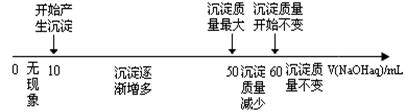
�����жϣ�������ͼ������������ܷ�����Ͻ���þ����������? (ѡ��ܡ����ܡ�)
���Т٢�����ѡһ������
������������Ͻ���þ��������������˵������ ��
����������Ͻ���þ��������������þ����������Ϊ ������һλС������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
��һ��NaCl��Na2CO3��10H2O��NaHCO3�Ļ���ijͬѧ�������ʵ�飬
ͨ��������Ӧǰ��C��Dװ�������ı仯���ⶨ�û�����и���ֵ�����������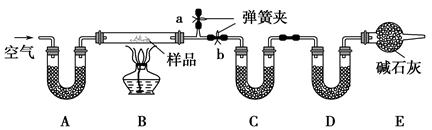
(1)����ǰͨ�������Ŀ���� ��
��������Ϊ ��
(2)װ��A��C��D��ʢ�ŵ��Լ��ֱ�Ϊ��A ��
C ��D ��
(3)����Aװ�û���ʢ��NaOH��Һ��ϴ��ƿ�����õ�NaCl�ĺ����� (�ƫ�ߡ�����ƫ�͡�����Ӱ�족����ͬ)����B�з�Ӧ���Ҳ���ˮ������������ⶨ�����NaHCO3�ĺ����� ������ȥEװ�ã�����Na2CO3��10H2O�ĺ����� ��
(4)����Ʒ����Ϊw g����Ӧ��C��D���ӵ������ֱ�Ϊm1 g��m2 g���ɴ˿�֪�������NaHCO3����������Ϊ (�ú�w��m1��m2�Ĵ���ʽ��ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�������Ũ�������ܷ����ۻ���ij��ȤС���ͬѧ���ֽ�һ����������Ũ�������ʱ���۲쵽����ȫ�ܽ⣬�������������塣ʵ�������������Լ���0.01 mol/L ����KMnO4��Һ��0.1 mol/L KI��Һ��3��H2O2��Һ��������Һ������ˮ������Э������̽��������Һ������ijɷ֡�
��������롿
��.������Һ�еĽ������ӿ��ܺ���Fe2+��Fe3+�е�һ�ֻ����֣�
��.���������п��ܺ���_________�е�һ�ֻ����֡�
| | ʵ����� | Ԥ������ | ���� |
| ��֤����� | ����٣�ȡ����0.01 mol/L����KMnO4��Һ������������Һ | | |
| ����ڣ�_________ | | ����Fe3�� | |
| ��֤����� | ����������ͨ������װ�� | | ������������ |

�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com