
(13分)
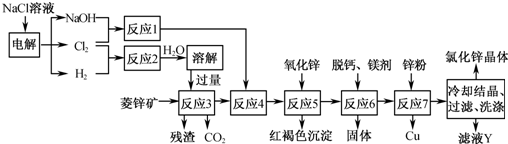
用菱锌矿(主要成分为碳酸锌,还含有Fe2+、Fe3+、Mg2+、Ca2+、Cu2+等)制备氯化锌的一种流程如下。

(1) 在反应3前要将菱锌矿研磨,其目的是。
(2) 反应4将Fe2+ 氧化为Fe3+,该反应的离子方程式为。
(3) 加入氧化锌调节至pH=4.5,反应5的离子方程式为。
(4) 锌粉不在反应4之前加入的原因是。
(5) 若用石墨做电极电解滤液Y,则可以得到参与本流程反应的物质有。
 期末集结号系列答案
期末集结号系列答案科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源:四川省绵阳中学2011届高三化学考前热点训练:14工艺流程、无机综合题 题型:022
用菱锌矿(主要成分为碳酸锌,还含有Fe2+.、Fe3+、Mg2+、Ca2+、Cu2+等)制备氯化锌的种流程如下.

(1)在反应3前要将菱锌矿研磨,其目的是________.
(2)反应4将Fe2+氧化为Fe3+,该反应的离子方程式为________.
(3)加入氧化锌调节pH==4.5,反应5的离子方程式为________.
(4)锌粉不在反应4之前加入的原因是________.
(5)若用石墨做电极电解滤液Y,则可以得到参与本流程反应的物质有________.
查看答案和解析>>
科目:高中化学 来源: 题型:
(13分)
用菱锌矿(主要成分为碳酸锌,还含有Fe2+、Fe3+、Mg2+、Ca2+、Cu2+等)制备氯化锌的一种流程如下。
(1) 在反应3前要将菱锌矿研磨,其目的是。
(2) 反应4将Fe2+ 氧化为Fe3+,该反应的离子方程式为。
(3) 加入氧化锌调节至pH=4.5,反应5的离子方程式为。
(4) 锌粉不在反应4之前加入的原因是。
(5) 若用石墨做电极电解滤液Y,则可以得到参与本流程反应的物质有。
查看答案和解析>>
科目:高中化学 来源:2012届四川省乐山市高三第二次调查研究考试理科综合试卷(化学部分) 题型:填空题
(13分)
用菱锌矿(主要成分为碳酸锌,还含有Fe2+、Fe3+、Mg2+、Ca2+、Cu2+等)制备氯化锌的一种流程如下。
(1) 在反应3前要将菱锌矿研磨,其目的是。
(2) 反应4将Fe2+ 氧化为Fe3+,该反应的离子方程式为。
(3) 加入氧化锌调节至pH=4.5,反应5的离子方程式为。
(4) 锌粉不在反应4之前加入的原因是。
(5) 若用石墨做电极电解滤液Y,则可以得到参与本流程反应的物质有。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com