
【题目】下列物质鉴别的方法可行的是( )
A. 用KMnO4 酸性溶液检验石蜡中是否有不饱和烃
B. 用石蕊试纸区别苯酚溶液和小苏打溶液
C. 用BaCl2 溶液区别硫酸和盐酸
D. 用Cu(OH)2 的碱性浊液区别甲醛溶液和乙醛溶液
科目:高中化学 来源: 题型:
【题目】甲~庚等元素在周期表中的相对位置如下表,己的最高氧化物对应水化物有强脱水性,甲和丁在同一周期,甲原子最外层与最内层具有相同电子数.下列判断正确的是( )
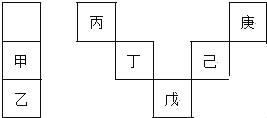
A. 丙与戊的原子序数相差28
B. 气态氢化物的稳定性:庚<己<戊
C. 常温下,庚和乙形成的化合物易溶于水
D. 丁的最高价氧化物不与任何酸反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列关于电极的说法正确的是
A. 铜电极只能作正极 B. 电解精炼铜时,纯铜与电源正极相连
C. 原电池的负极得到电子 D. 电解池的阳极失去电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】根据题意回答问题:
(1)中和热的测定所需的玻璃仪器有:大小烧杯、量筒、温度计、 ;
已知:0.55 mol·L-1 HCl和0.50 mol·L-1的NaOH溶液各50 mL反应放出热量为1.42kJ,写出该反应的中和热的热化学方程式: 。
(2)101kpa时,1克乙醇(CH3CH2OH)液体完全燃烧生成稳定氧化物放出热量akJ,写出乙醇燃烧热的热化学方程式: 。
(3)已知H-H、O=O和O-H键的键能分别为436 kJ/mol、498 kJ/mol和463 kJ/mol,2H2O(g) = 2H2(g)+ O2(g) ΔH2= 。
(4)用CO2和氢气合成CH3OCH3(甲醚)是解决能源危机的研究方向之一。
已知:CO(g)+2H2(g ![]() CH3OH(g) ΔH=-90.7 kJ·mol-1
CH3OH(g) ΔH=-90.7 kJ·mol-1
2CH3OH(g ![]() CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CH3OCH3(g)+H2O(g) ΔH=-23.5 kJ·mol-1
CO(g)+H2O(g ![]() CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
CO2(g)+H2(g) ΔH=-41.2 kJ·mol-1
则CO2和氢气合成CH3OCH3(g)的热化学方程式为: 。
(5)① 25℃时,浓度均为0.1 mol/L的①氨水②氢氧化钠溶液③盐酸溶液④醋酸溶液,其c(H+)由大到小排列的顺序为: (用序号填空)。
② 95℃时,水中的H+的物质的量浓度为10-6 mol·L-1,若把0.01 mol的NaOH固体溶解于95℃水中配成1 L溶液,则溶液的pH为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】.下列叙述正确的是(用NA代表阿伏加德罗常数的值) ( )
A. 1.8gD2O中所含中子数为NA
B. 7.8gNa2O2与足量水反应电子转移0.2NA
C. 在标准状况下,22.4LCH4与18gH2O所含有的电子数均为10 NA
D. 1.6gO2与O3混合气体中所含O原子数目为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表为元素周期表的一部分,请回答有关问题:
ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
2 | ① | ② | ||||||
3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ||
4 | ⑨ | ⑩ |
(1)表中最活泼的金属元素是____(填写元素符号,以下同),非金属性最强的元素是_____;
(2)③与④的最高价氧化物对应水化物的碱性较弱的是__________(填写化学式)。
(3)工业制取⑤的单质的化学反应方程式为:____________________。⑤的气态氢化物在空气中燃烧生成两种氧化物,写出该反应的化学方程式:______________。
(4)写出一个能比较⑦、⑩单质氧化性强弱的离子方程式:________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列试剂的保存方法,错误的是( )
A.把浓硝酸放在棕色瓶中,并置于冷暗处保存
B.把Na保存在煤油中
C.把NaOH溶液放在带橡皮塞的玻璃瓶中
D.把氢氟酸放在玻璃瓶中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某课外小组准备在实验室配制100mL1.0mol·L-1的硝酸溶液,然后再研究金属铜与硝酸的反应情况。
(1)配制100mL1.0mol·L-1的硝酸溶液,需要的仪器除烧杯、玻璃棒、量筒、胶头滴管外,还需要的玻璃仪器是______________________。
(2)若用10 mol·L-1的浓硝酸来配制上述溶液,需要量取浓硝酸的体积是_______mL。
(3)配制过程中,若其他操作都正确,下列操作会引起浓度偏小的是__________。
A.定容摇匀后发现液面低于刻度线,再加水至刻度线
B.定容时俯视容量瓶的刻度线
C.将溶液转入容量瓶后,没有洗涤烧杯和玻璃棒,就进行定容操作
D.容量瓶用蒸馏水洗涤后未烘干
(4)课外小组同学将制得的硝酸与铜片在下列装置中反应,反应初期观察到大试管中的液体a逐渐变为蓝色,试管上方有浅红棕色气体出现。
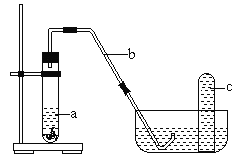
① 反应初期液体a逐渐变为蓝色是由于反应生成了____________(填化学式)。
② 导致红棕色气体在试管c中颜色消失的反应方程式为____________________。
③ 你能否通过该实验初期现象得出1.0mol·L-1的硝酸与铜片反应直接生成红棕色NO2的结论?_________(填“能”或“不能”),理由是 __________________________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com