
| A�� | �����ϲ����ܹ�ʹʪ����۵⻯����ֽ���������� | |
| B�� | ���һ��ʱ����ص��¶�����10�棬��ʱ��Ƭ��������������ʼӿ� | |
| C�� | ���ʱ��������ͭƬ�缫�����ƶ� | |
| D�� | ���һ��ʱ�����Һ�л������ɫ�������ܷ�ӦΪ��Cu+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$Cu��OH��2��+H2�� |
���� ������ȵ���Ƭ��ͭƬ�����Ȼ�����Һ�У�ͭƬ���Դ����������Ϊ��������������Ӧ����ӦʽΪ��Cu-2e-=Cu2+����Ƭ���Դ�ĸ�������Ϊ����������ԭ��Ӧ����ӦʽΪ��2H++2e-=H2�����ݴ˷�����
��� �⣺A��ͭƬ���Դ����������Ϊ��������������Ӧ����ӦʽΪ��Cu-2e-=Cu2+������û�в����ܹ�ʹʪ����۵⻯����ֽ���������壬��A����
B�����ص��¶�����10�棬��Ӧ���ʼӿ죬������Ƭ��������������ʼӿ죬��B��ȷ��
C����������������Ƭ�缫�����ƶ�����C����
D��ͭƬ���Դ����������Ϊ��������������Ӧ����ӦʽΪ��Cu-2e-=Cu2+����Ƭ���Դ�ĸ�������Ϊ����������ԭ��Ӧ����ӦʽΪ��2H++2e-=H2�������Ե��һ��ʱ�����Һ�л������ɫ�������ܷ�ӦΪ��Cu+2H2O$\frac{\underline{\;ͨ��\;}}{\;}$Cu��OH��2��+H2������D��ȷ��
��ѡBD��
���� ���⿼���˵��ص�ԭ�����ѶȲ�����ȷ���������жϷ�������缫��Ӧʽ�ǽⱾ��Ĺؼ���


 ����ѧ��ţ��Ӣ��ϵ�д�
����ѧ��ţ��Ӣ��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���³�ѹ�µ�33.6L������27g����ַ�Ӧ��ת�Ƶ�����Ϊ3NA | |
| B�� | 7.8g Na2O2��������������������Ϊ0.4NA | |
| C�� | ��CO2��O2��ɵĻ�����й���NA�����ӣ����е���ԭ����Ϊ2NA | |
| D�� | 1LŨ��Ϊ1mol•L-1��Na2CO3��Һ�к���NA��CO${\;}_{3}^{2-}$ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | O2��O3��Ϊͬλ�� | B�� | O2��O3���ת���ǻ�ѧ�仯 | ||
| C�� | O3����3����ԭ�ӹ��ɵĻ����� | D�� | ������O2��O3���е�����������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 1��2 | B�� | 2��3 | C�� | 3��2 | D�� | 1��1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ˮ�����������͵�ԭ��������ˮ�����ڴ��������ɵ� | |
| B�� | F2��Cl2��Br2��I2������ɽṹ���ƣ���Է��������������Ӽ������������������۷е������� | |
| C�� | ����Ԫ�����ڱ���֪ʶ�ж�51Sb��һ�ֿ�����Ϊ�뵼����ϵķǽ���Ԫ�� | |
| D�� | ̼Ԫ���ж��ֺ��أ���12C��13C��14C��C60���ǻ�Ϊͬλ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������


 ��
�� ��
�� $?_{��}^{Ũ����}$
$?_{��}^{Ũ����}$ +��2n-1��H2O��
+��2n-1��H2O�� ��
�� ��
�� ��
�� ��
���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | ICl�������ӻ�������н�ǿ�������� | |
| B�� | �����ʵ�����Cl2��ICl�����������ʵ�����SO2 | |
| C�� | ICl��ˮ��Ӧ������������ԭ��Ӧ | |
| D�� | ICl������������Һ��Ӧ������NaI��NaClO |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
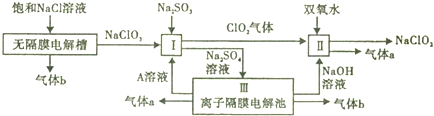
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com