
【题目】(1)0.6mol O2与0.4mol O3的质量之比为______,分子个数之比为_______,O原子的物质的量之比为______。
(2)49g硫酸是_______mol,含有______mol O,电离可产生______个氢离子。
【答案】1:1 3:2 1:1 0.5 2.0 NA
【解析】
(1)根据m=n·M计算两种物质的质量比;根据N=n·NA计算分子个数关系;结合微粒中构成微粒与物质的量计算;
(2)根据n=![]() 计算硫酸的物质的量,根据n(O)=4n(H2SO4)计算,n(H+)=2n(H2SO4)和N=n·NA计算氢离子个数。
计算硫酸的物质的量,根据n(O)=4n(H2SO4)计算,n(H+)=2n(H2SO4)和N=n·NA计算氢离子个数。
(1)m(O2)=0.6mol×32g/mol=19.2g,m(O3)=0.4mol×48g/mol=19.2g,0.6mol O2与0.4mol O3的质量相等,故m(O2):m(O3)=1:1;根据N=n·NA可知N(O2)=0.6NA;N(O3)=0.4NA,所以N(O2):N(O3)=3:2;0.6mol O2中含有1.2molO原子;0.4mol O3中含有O原子的物质的量是1.2mol,二者含有O原子的物质的量相等,因此两种气体中含有的O原子的物质的量之比为1:1;
(2)n(H2SO4)=49g÷98g/mol=0.5mol;n(O)=4n(H2SO4)=4×0.5mol=2.0mol,n(H+)=2n(H2SO4)=2×0.5mol=1.0mol,氢离子个数是N=n·NA=1mol×NA/mol=NA。


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】室温下,反应![]() +H2O
+H2O![]() H2CO3+OH的平衡常数K=2.2×108。将NH4HCO3溶液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒物质的量浓度关系正确的是
H2CO3+OH的平衡常数K=2.2×108。将NH4HCO3溶液和氨水按一定比例混合,可用于浸取废渣中的ZnO。若溶液混合引起的体积变化可忽略,室温时下列指定溶液中微粒物质的量浓度关系正确的是
A. 0.2mol·L1氨水:c(NH3·H2O)>c(![]() )>c(OH)>c(H+)
)>c(OH)>c(H+)
B. 0.2mol·L1NH4HCO3溶液(pH>7):c(![]() )>c(
)>c(![]() )>c(H2CO3)>c(NH3·H2O)
)>c(H2CO3)>c(NH3·H2O)
C. 0.2mol·L1氨水和0.2mol·L1NH4HCO3溶液等体积混合:c(![]() )+c(NH3·H2O)=c(H2CO3)+c(
)+c(NH3·H2O)=c(H2CO3)+c(![]() )+c(
)+c(![]() )
)
D. 0.6mol·L1氨水和0.2mol·L1NH4HCO3溶液等体积混合:c(NH3·H2O)+c(![]() )+c(OH)=0.3mol·L1+c(H2CO3)+c(H+)
)+c(OH)=0.3mol·L1+c(H2CO3)+c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )
A. 有机物(![]() )的名称为2-甲基-1-丙醇
)的名称为2-甲基-1-丙醇
B. 芥子醇( )能发生氧化、取代、水解、加聚反应
)能发生氧化、取代、水解、加聚反应
C. 1mol绿原酸( )与足量溴水反应,最多消耗4molBr2
)与足量溴水反应,最多消耗4molBr2
D. 有机物(俗称“一滴香”)( )的一种含苯环的同分异构体能发生银镜反应
)的一种含苯环的同分异构体能发生银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上以CO和H2为原料合成甲醇的反应:CO(g)+2H2(g)![]() CH3OH(g) △H<0,在容积为1 L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。右图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是
CH3OH(g) △H<0,在容积为1 L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。右图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为1mol)与CO平衡转化率的关系。下列说法正确的是
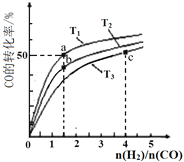
A. H2转化率:a>b>c
B. 上述三种温度之间关系为T1>T2>T3
C. a点状态下再通入0.5 mol CO和0.5 mol CH3OH,平衡向正方向移动
D. c点状态下再通入1 molCO和4 mol H2,新平衡中CH3OH的体积分数增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氟苯水杨酸(diflunisal)是一种新型的水杨酸类消炎解热镇痛良药,具有强效、长效低毒等特点。一种可行的合成路线如下(催化剂及溶剂等已省去):
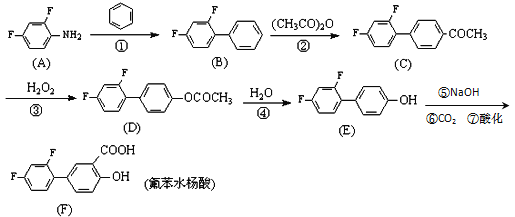
试回答下列问题:
(1)有关氟苯水杨酸的下列说法正确的是______________(选填序号)。
A 分子中只含两种官能团
B 分子中所有原子可以处于同一平面(已知:HCOOH所有原子可在同一平面)
C 1mol氟苯水杨酸与足量的碳酸氢钠溶液反应,可生成2molCO2
D 在一定pH条件下,氟苯水杨酸遇FeCl3溶液能发生显色反应
E 在一定条件下,氟苯水杨酸能发生取代反应
(2)图中有机物(A)为2,4-二氟苯胺,它的化学式为_______。A的同分异构体中,含有苯环且与A具有相同官能团的同分异构体有_____种(不包括A)。
(3)上述①②③④反应中属于取代反应的有:_________。
(4)反应②的方程式为:____________________________。(不需注明反应条件)
(5)反应③有2种生成物,另一种生成物是无机物,其化学式为______
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮元素是造成水体富营养化的主要原因,在水中常以氨氮或NO3形式存在。
(1)在pH为4~6时,用H2在Pd-Cu催化下将NO3-还原为N2可消除水中NO3。该反应的离子方程式为____。若用H2和CO2的混合气体代替H2,NO3-去除效果更好,其原因是____。
(2)NaClO氧化可除去氨氮,反应机理如图1所示(其中H2O和NaCl略去),实验测得相同条件下,相同反应时间,pH与氨氮的去除率关系如图2所示,温度与氨氮去除率关系如图3所示。



图1 图2 图3
①NaClO氧化NH3的总反应的化学方程式为____。
②如图2所示,在pH>9时,pH越大去除率越小,其原因是____。
③如图3所示,温度低于15℃时,温度越低去除率越低其原因是____。当温度高于25℃时,温度越高去除率也越低,其原因是____。
(3)用电化学法可去除废水中的氨氮。在含NH4+的废水中加入氯化钠,用惰性电极电解。反应装置如图4所示,则电解时,a极的电极反应式为____。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用阳极X和阴极Y电解足量Z的水溶液,电解一段时间后,再加入W,能使溶液恢复到电解前的状态,符合题意的一组是( )
选项 | 阳极X | 阴极Y | Z | W |
A | C | Fe | KCl | KOH |
B | Pt | Cu | CuSO4 | Cu(OH)2溶液 |
C | C | C | H2SO4 | H2O |
D | Ag | Fe | AgNO3 | AgNO3晶体 |
A. AB. BC. CD. D
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁和钴是两种重要的过渡元素。请回答下列问题:
(1)钴在元素周期表中的位置是___________,其基态原子的价电子排布图为___________。
(2)FeCO3是菱铁矿的主要成分,其中C原子的杂化方式为________;分子中的大π键可用符号Π![]() 表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π
表示,其中m代表参与形成大π键的原子数,n代表参与形成大π键的电子数(如苯分子中的大π键可表示为Π![]() ),则CO32-中的大π键应表示为________。
),则CO32-中的大π键应表示为________。
(3)已知Fe2+半径为61pm,Co2+半径为65pm,在隔绝空气条件下分别加热FeCO3和CoCO3,实验测得FeCO3受热分解温度低于CoCO3,其原因可能是______。
(4)Co(NH3)5Cl3是钴的一种配合物,向含0.01mol该配合物的溶液中加入足量AgNO3溶液,生成白色沉淀2.87g。则该配合物的配位数为_____。
(5)奥氏体是碳溶解在r-Fe中形成的一种间隙固溶体,无磁性,其晶胞为面心立方结构(如图所示),则该晶体中与铁原子距离最近的铁原子数目为___________;若该晶胞参数为a pm,则该晶体的密度为___________g·cm-3(阿伏加德罗常数的值用NA表示)。
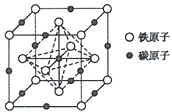
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C、X均为中学化学常见物质,一定条件下它们有如图所示转化关系(部分产物已略去)。下列说法正确的是( )
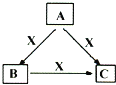
A. 若X为KOH溶液,则A可能为Al
B. 若X为Fe,则C可能为Fe(NO3)2溶液
C. 若A、B、C均为焰色反应呈黄色的化合物,则X一定为CO2
D. 若X为O2,则A可为有机物乙醇,也可为非金属单质硫
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com