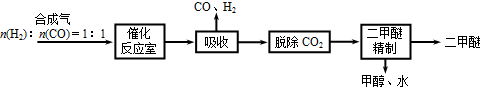
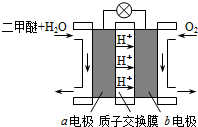
(2011?如皋市模拟)金属镍及其化合物在合金材料以及催化剂等方面应用广泛.目前,全世界镍的消费量仅次于铜、铝、铅、锌,居有色金属第五位,镍行业发展蕴藏着巨大的潜力.
(1)基态Ni原子的核外电子排布式为
1s22s22p63s23p63d84s2
1s22s22p63s23p63d84s2
.
(2)金属镍能与CO形成配合物Ni(CO)
4,写出与CO互为等电子体的一种分子和一种离子的化学式为
N2;CN-
N2;CN-
.
(3)很多不饱和有机物在Ni催化下可与H
2发生加成反应.如①CH
2=CH
2、②HC≡CH、③

、④HCHO等,其中碳原子采取sp
2杂化的分子有
①③④
①③④
(填物质序号),预测HCHO分子的立体结构为
平面三角
平面三角
形.
(4)NiO的晶体结构类型与氯化钠的相同,NiO晶胞中Ni和O的配位数分别为
6
6
;Ni
2+和Fe
2+的离子半径分别为69pm和78pm,则熔点NiO
>
>
FeO(填“<”或“>”);
(5)金属镍与镧(La)形成的合金是一种良好的储氢材料,其晶胞结构示意图如左下图所示.该合金的化学式为
LaNi5或Ni5La
LaNi5或Ni5La
;

(6)丁二酮肟常用于检验Ni
2+:在稀氨水介质中,丁二酮肟与Ni
2+反应可生成鲜红色沉淀,其结构如图所示.该结构中,除共价键外还存在配位键和氢键,请在图中用箭头和“…”表示出配位键和氢键
.

 、④HCHO等,其中碳原子采取sp2杂化的分子有
、④HCHO等,其中碳原子采取sp2杂化的分子有


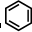 中每个碳原子含有3个σ键,不含孤电子对,所以采取sp2杂化,故正确;
中每个碳原子含有3个σ键,不含孤电子对,所以采取sp2杂化,故正确; ,故答案为:
,故答案为: .
.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案