
ƽ��ָ���������෴����ı仯����������˶�״̬;��ѧ���漰��ƽ������
����淴Ӧ��ƽ�⡢������ƽ�⡢ˮ��ƽ�⼰�������ܽ�ƽ��ȵȡ�
(1)�����ݻ�Ϊ2L�ĺ��º����ܱ������������м���2molA�����2molB�����
�����·�Ӧ�� A(g)ʮB(g)![]() C(g)
C(g) ![]()
20s��Ӧ�ﵽƽ��״̬������lmolC���壬�ų�����Q1kJ���ش��������⡣
�ټ��� 20s��B�����ƽ����ѧ��Ӧ����Ϊ ������÷�Ӧ��ƽ�ⳣ��
��
�ڱ��������¶Ⱥ��ݻ����䣬����Ϊ�����м���1molC���壬��Ӧ�ﵽƽ��ʱ����������QkJ����Q1��Q2�����ϵ��ȷ���� ������ĸ����
(A)Ql+Q2=a (B)Q1+2Q2<2a (C) Q1+2Q2>2a (D) Ql+Q2<a
(2)�״���һ�ֿ�������Դ�����п�����Ӧ�õĹ���ǰ������ҵ�Ͽ��úϳ����Ʊ��״�����ӦΪCO(g)+2H2(g)![]() CH3OH(g)ij�¶��£����ݻ�Ϊ2L���ܱ������н��и÷�Ӧ������� ��������ݼ���ͼ��
CH3OH(g)ij�¶��£����ݻ�Ϊ2L���ܱ������н��и÷�Ӧ������� ��������ݼ���ͼ��

��tmin��2tminʱ���ʱ仯��ԭ������� ��
��3tminʱ�Է�Ӧ��ϵ��ȡ��һ����ʩ����4tminʱCO�����ʵ���Ϊ0.5mol���������ͼCO�ı仯���ߡ�
(3)�����£���VmL��0.1000mol��L-1����������Һ��μ��뵽20.00mol��L-1����
��Һ�У���ַ�Ӧ���ش��������⡣(������Һ����ı仯)
�������ҺpH=7����ʱV��ȡֵ 20.00(�>������<����=")������Һ�С�c(Na+)��
��![]() �Ĵ�С��ϵ;
�Ĵ�С��ϵ;
��
���� �� V=40.00���� �� ʱ ��Һ �� ![]()
mol��L-1
(4)ij�¶������£�����CO2(g)��H2(g)�������1:4��ϣ����ʵ�ѹǿ�ʹ���
�����¿��Ƶü��飬��֪:
![]()
��CO2(g)��H2(g)��Ӧ����Һ̬ˮ���Ȼ�ѧ����ʽΪ:
 ��������һ���þ�ϵ�д�
��������һ���þ�ϵ�д� Сѧ��10����Ӧ����ϵ�д�
Сѧ��10����Ӧ����ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| c(C) |
| c(A)?c(B) |
| c(C) |
| c(A)?c(B) |
| 1 |
| 3 |
| 1 |
| 30 |
| 1 |
| 30 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013�콭��ʡ̩����ѧ������ѧ�����п��Ի�ѧ�Ծ����������� ���ͣ������
��15�֣�ƽ��ָ���������෴����ı仯����������˶�״̬����ƽ��ʱ�����ֱ仯���ڼ������У��������ǵ�������ȣ����ݱ仯�����ʿɷ�Ϊ����ƽ��ͻ�ѧƽ�⣬��ѧ���漰��ƽ����������淴Ӧ��ƽ�⡢������ƽ�⡢ˮ��ƽ�⼰�������ܽ�ƽ��ȵȡ�
��1�������ݻ�Ϊ1 L�ĺ��º����ܱ������������м���2 mol A�����2 mol B����������·�Ӧ��A(g)��B(g) C(g) ��H=" -" a kJ��mol-1��20s��Ӧ�ﵽƽ��״̬������1 mol C���壬�ų�����Q1kJ���ش��������⡣
C(g) ��H=" -" a kJ��mol-1��20s��Ӧ�ﵽƽ��״̬������1 mol C���壬�ų�����Q1kJ���ش��������⡣
�ټ���20s��B�����ƽ����ѧ��Ӧ����Ϊ___________��д���÷�Ӧ��ƽ�ⳣ������ʽ___________��
�ڱ��������¶Ⱥ��ݻ����䣬����Ϊ�����м���1molC���壬��Ӧ�ﵽƽ��ʱ����������Q2kJ����Q1 ��Q2�����ϵ��ȷ����____________������ĸ����
��A��Q1 + Q2 = a ��B�� Q1 + 2Q2 < 2a ��C��Q1 + 2Q2 > 2a ��D��Q1 + Q2 < a
����ԭƽ������ϣ����������¶Ⱥ��ݻ����䣬����������ͨ��bmolA���壨b>0��ʱ��v(��)_____v(��)���>������<����=���������´�ƽ���C�����ƽ��������� (C) =
(C) = 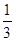 ����b = ____________��
����b = ____________��
��2�������£���VmL��0.1000mol��L-1����������Һ��μ��뵽20.00mL��0.1000mol��L-1������Һ�У���ַ�Ӧ���ش��������⡣��������Һ����ı仯��
�������ҺpH=7����ʱV��ȡֵ_____20.00���>������<����=����������Һ��c(Na+)��c(CH3COO-)��c(H+)��c(OH-)�Ĵ�С��ϵΪ_____________________________________________��
�����V=40.00�����ʱ��Һ��c(OH��) -c(H��) - c(CH3COOH)= ___________________mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2013��ɽ��ʡ��������̨һ�и�����ѧ�����п��Ի�ѧ�Ծ����������� ���ͣ������
��16�֣�ƽ��ָ���������෴����ı仯����������˶�״̬����ƽ��ʱ�����ֱ仯���ڼ������У��������ǵ�������ȣ����ݱ仯�����ʿɷ�Ϊ����ƽ��ͻ�ѧƽ�⣬��ѧ���漰��ƽ����������淴Ӧ��ƽ�⡢������ƽ�⡢ˮ��ƽ�⼰�������ܽ�ƽ��ȵȡ�
��1�������ݻ�Ϊ1 L�ĺ��º����ܱ������������м���2 mol A�����2 mol B����������·�Ӧ��
A(g) �� B(g)  C(g) ��H= - a kJ��mol-1
C(g) ��H= - a kJ��mol-1
20s��Ӧ�ﵽƽ��״̬������1 mol C���壬�ų�����Q1kJ���ش��������⡣
�ټ���20s��B�����ƽ����ѧ��Ӧ����Ϊ___________��д���÷�Ӧ��ƽ�ⳣ������ʽ___________��
�ڱ��������¶Ⱥ��ݻ����䣬����Ϊ�����м���1molC���壬��Ӧ�ﵽƽ��ʱ����������Q2kJ����Q1 ��Q2�����ϵ��ȷ����____________������ĸ����
��A��Q1 + Q2 = a ��B�� Q1 + 2Q2 < 2a ��C��Q1 + 2Q2 > 2a ��D��Q1 + Q2 < a
����ԭƽ������ϣ����������¶Ⱥ��ݻ����䣬����������ͨ��b mol A���壨b>0��ʱ��v(��)_____v(��)���>������<����=���������´�ƽ���C�����ƽ��������� (C) =
(C) = 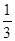 ����b = ____________��
����b = ____________��
��2�������£���VmL��0.1000mol��L-1����������Һ��μ��뵽20.00mL��0.1000mol��L-1������Һ�У���ַ�Ӧ���ش��������⡣��������Һ����ı仯��
�������ҺpH=7����ʱV��ȡֵ_____20.00���>������<����=����������Һ��c(Na��)��c(CH3COO��)��c(H��)��c(OH��)�Ĵ�С��ϵΪ_____________________________________________��
�����V=40.00�����ʱ��Һ��c(OH��) - c(H��) - c(CH3COOH)= ___________________mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ�꽭��ʡ������ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��15�֣�ƽ��ָ���������෴����ı仯����������˶�״̬����ƽ��ʱ�����ֱ仯���ڼ������У��������ǵ�������ȣ����ݱ仯�����ʿɷ�Ϊ����ƽ��ͻ�ѧƽ�⣬��ѧ���漰��ƽ����������淴Ӧ��ƽ�⡢������ƽ�⡢ˮ��ƽ�⼰�������ܽ�ƽ��ȵȡ�
��1�������ݻ�Ϊ1 L�ĺ��º����ܱ������������м���2 mol A�����2 mol B����������·�Ӧ��A(g)��B(g) C(g) ��H= - a kJ��mol-1��20s��Ӧ�ﵽƽ��״̬������1 mol C���壬�ų�����Q1kJ���ش��������⡣
C(g) ��H= - a kJ��mol-1��20s��Ӧ�ﵽƽ��״̬������1 mol C���壬�ų�����Q1kJ���ش��������⡣
�ټ���20s��B�����ƽ����ѧ��Ӧ����Ϊ___________��д���÷�Ӧ��ƽ�ⳣ������ʽ___________��
�ڱ��������¶Ⱥ��ݻ����䣬����Ϊ�����м���1molC���壬��Ӧ�ﵽƽ��ʱ����������Q2kJ����Q1 ��Q2�����ϵ��ȷ����____________������ĸ����
��A��Q1 + Q2 = a ��B�� Q1 + 2Q2 < 2a ��C��Q1 + 2Q2 > 2a ��D��Q1 + Q2 < a
����ԭƽ������ϣ����������¶Ⱥ��ݻ����䣬����������ͨ��bmolA���壨b>0��ʱ��v(��)_____v(��)���>������<����=���������´�ƽ���C�����ƽ���������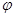 (C) =
(C) = 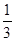 ����b = ____________��
����b = ____________��
��2�������£���VmL��0.1000mol��L-1����������Һ��μ��뵽20.00mL��0.1000mol��L-1������Һ�У���ַ�Ӧ���ش��������⡣��������Һ����ı仯��
�������ҺpH=7����ʱV��ȡֵ_____20.00���>������<����=����������Һ��c(Na+)��c(CH3COO-)�� c(H+)��c(OH-)�Ĵ�С��ϵΪ_____________________________________________��
�����V=40.00�����ʱ��Һ��c(OH��) -c(H��) - c(CH3COOH)= ___________________mol��L-1��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2012-2013ѧ��ɽ��ʡ�����и�����ѧ�����п��Ի�ѧ�Ծ��������棩 ���ͣ������
��16�֣�ƽ��ָ���������෴����ı仯����������˶�״̬����ƽ��ʱ�����ֱ仯���ڼ������У��������ǵ�������ȣ����ݱ仯�����ʿɷ�Ϊ����ƽ��ͻ�ѧƽ�⣬��ѧ���漰��ƽ����������淴Ӧ��ƽ�⡢������ƽ�⡢ˮ��ƽ�⼰�������ܽ�ƽ��ȵȡ�
��1�������ݻ�Ϊ1 L�ĺ��º����ܱ������������м���2 mol A�����2 mol B����������·�Ӧ��
A(g) �� B(g)  C(g) ��H=
- a kJ��mol-1
C(g) ��H=
- a kJ��mol-1
20s��Ӧ�ﵽƽ��״̬������1 mol C���壬�ų�����Q1kJ���ش��������⡣
�ټ���20s��B�����ƽ����ѧ��Ӧ����Ϊ___________��д���÷�Ӧ��ƽ�ⳣ������ʽ___________��
�ڱ��������¶Ⱥ��ݻ����䣬����Ϊ�����м���1molC���壬��Ӧ�ﵽƽ��ʱ����������Q2kJ����Q1 ��Q2�����ϵ��ȷ����____________������ĸ����
��A��Q1 + Q2 = a ��B�� Q1 + 2Q2 < 2a ��C��Q1 + 2Q2 > 2a ��D��Q1 + Q2 < a
����ԭƽ������ϣ����������¶Ⱥ��ݻ����䣬����������ͨ��b mol A���壨b>0��ʱ��v(��)_____v(��)���>������<����=���������´�ƽ���C�����ƽ���������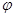 (C)
=
(C)
= 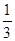 ����b
= ____________��
����b
= ____________��
��2�������£���VmL��0.1000mol��L-1����������Һ��μ��뵽20.00mL��0.1000mol��L-1������Һ�У���ַ�Ӧ���ش��������⡣��������Һ����ı仯��
�������ҺpH=7����ʱV��ȡֵ_____20.00���>������<����=����������Һ��c(Na��)��c(CH3COO��)�� c(H��)��c(OH��)�Ĵ�С��ϵΪ_____________________________________________��
�����V=40.00�����ʱ��Һ��c(OH��) - c(H��) - c(CH3COOH)= ___________________mol��L-1��
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com