
由气态基态原子形成1mol化学键释放的最低能量叫键能。从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量。已知反应N2+3H2 ![]() 2NH3 △H=a kJ?mol-1。试根据表中所列键能数据估算a 的数值: 。
2NH3 △H=a kJ?mol-1。试根据表中所列键能数据估算a 的数值: 。
![]()
 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案科目:高中化学 来源: 题型:
| 化学键 | H-H | N-H | N≡N |
| 键能/kJ?mol-1 | 436 | 391 | 946 |
查看答案和解析>>
科目:高中化学 来源:福建省福州八县(市)一中2011-2012学年高二上学期期中联考化学理科试题 题型:022
为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施.化学反应的反应热通常用实验进行测定,也可进行理论推算.
(1)今有如下两个热化学方程式:?则
a________b(填>,=,<)H2(g)+![]() O2(g)=H2O(g)
O2(g)=H2O(g)
H2(g)+![]() O2(g)=H2O(l) ΔH2=b kJ·mol-1
O2(g)=H2O(l) ΔH2=b kJ·mol-1
(2)由气态基态原子形成1 mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.

已知反应N2(g)+3H2(g)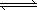 2NH3(g) ΔH=a kJ·mol-1.试根据表中所列键能数据估算a的值:________.
2NH3(g) ΔH=a kJ·mol-1.试根据表中所列键能数据估算a的值:________.
(3)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算.
已知:C(s)+O2(g)=CO2(g) ΔH1=-393
.5 kJ·mol-12H2(g)+O2(g)=2H2O(l) ΔH2=-571.6 kJ·mol-1
2C2H2(g)+5O2(g) 4CO2(g)+2H2O(l) ΔH3=-2599 kJ·mol-1
4CO2(g)+2H2O(l) ΔH3=-2599 kJ·mol-1
根据盖斯定律
,计算298 K时由C(s)和H2(g)生成1 mol C2H2(g)反应的反应热ΔH=________.查看答案和解析>>
科目:高中化学 来源:江苏省上冈高级中学2011-2012学年高二下学期期中考试化学试题 题型:022
为了合理利用化学能,确保安全生产,化工设计需要充分考虑化学反应的反应热,并采取相应措施.化学反应的反应热通常用实验进行测定,也可进行理论推算.
(1)实验测得,5 g甲醇在氧气中充分燃烧生成二氧化碳气体和液态水时释放出113.5 kJ的热量,则甲醇的燃烧热ΔH=________.
(2)今有如下两个热化学方程式:?则a________b(填>,=,<)
H2(g)+(3)由气态基态原子形成1 mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.
![]()
已知反应N2(g)+3H2(g)![]() 2NH3(g) ΔH=a kJ·mol-1.试根据表中所列键能数据估算a的值:________(写出+或-).
2NH3(g) ΔH=a kJ·mol-1.试根据表中所列键能数据估算a的值:________(写出+或-).
(4)依据盖斯定律可以对某些难以通过实验直接测定的化学反应的反应热进行推算.
已知:C(s)+O2(g)=CO2(g) ΔH1=-393.5kJ·mol-1
2H2(g)+O2(g)=2H2O(l) ΔH2=-571.6kJ·mol-1
2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH3=-2599kJ·mol-1
根据盖斯定律,计算298 K时由C(s)和H2(g)生成1 mol C2H2(g)反应的反应热ΔH=________.
查看答案和解析>>
科目:高中化学 来源:学习周报 化学 人教课标高二版(选修4) 2009-2010学年 第1期 总第157期 人教课标版(选修4) 题型:038
化学反应的焓变通常用实验进行测定,也可进行理论推算.
由气态基态原子形成
1 mol化学键释放的最低能量叫键能.从化学键的角度分析,化学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程.在化学反应过程中,拆开化学键需要消耗能量,形成化学键又会释放能量.已知,
CH3-CH3→CH2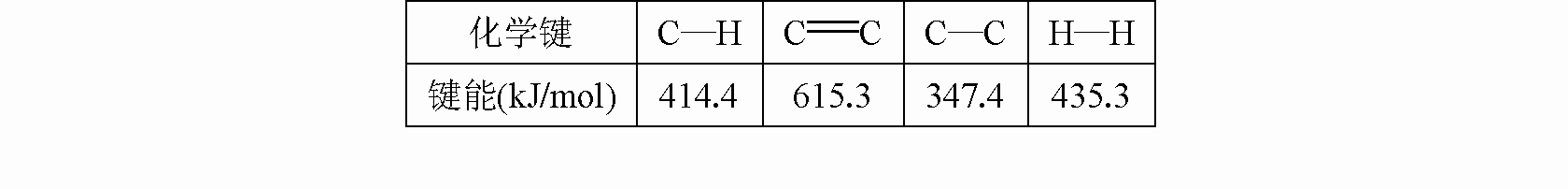
试计算该反应的反应热.
查看答案和解析>>
科目:高中化学 来源:2015届江苏常州市高二上学期第四次月考化学试卷(解析版) 题型:选择题
氮是地球上含量丰富的一种元素,氮及其化合物在工农业生产、生活中有着重要作用。请回答下列问题:
(1)右图是N2和H2反应生成2 mol NH3过程中能量变
化示意图,写出生成NH3的热化学方程式:
_____________________________________________
___________________________。
(2)由气态基态原子形成1 mol化学键释放的最低能量叫键能。从化学键的角度分析,化
学反应的过程就是反应物的化学键的破坏和生成物的化学键的形成过程。在化学反应过
程中,拆开化学键需要消耗能量,形成化学键又会释放能量。
已知反应N2(g)+3H2(g)??2NH3(g) ΔH=a kJ·mol-1。
试根据表中所列键能数据估算a的数值:________。
|
化学键 |
H—H |
N—H |
N≡N |
|
键能kJ·mol-1 |
436 |
391 |
945 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com