


 ȫ��������ϵ�д�
ȫ��������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���٢ܢݢ� | B���ڢݢޢ� |
| C���٢ۢݢ� | D���٢ۢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��0.1 mol?L-1NaOH��Һ��0.2 mol?L-1CH3COOH��Һ�������Ϻ�c��CH3COOH��+c��CH3COO-��=0.2 mol?L-1 |
| B�������£���CH3COONa��HCl����Һ��ϳ����Ե���Һ�У�c��Na+����c��Cl-��=c��CH3COOH�� |
| C��pH��ȵĢ�NH4Cl���ڣ�NH4��2SO4����NH4HSO4��Һ��c��NH4+����С˳��Ϊ��=�ڣ��� |
| D��25��ʱ��pH=a��������pH=b��Ba��OH��2��Һ�������Ϻ�ǡ����ȫ��Ӧ����a+b=14 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A������ʳƷ���Ӽ���ʳ������彡�����к� |
| B����ͨ�����͵������մɶ������������ǽ������� |
| C�������ƹ�Ӧ��ȼ�ϡ������������������ɼ�����������͵�������Կ�������Ⱦ |
| D��Ϊ������ȱ�����������涨��ʳ���б�������һ������KI |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A��ͬ����Ԫ�غ������������˵���������Ӷ����� |
| B����������Ų���ͬ������ѧ����Ҳ��ͬ |
| C��Cl-��S2-��Ca2+��K+�뾶��С |
| D��1735 Cl �� 1737 Cl �õ���������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
 ������CO2Ũ�ȵij����߸��Ѿ��������ǵĸ߶����ӣ���ѧ����ָ�������ж�����̼�ij�������������ʹȫ���ů�������ȫ�ı��ź�ˮ���ܽ����̼��CO2��HCO3-��CO32-����Ũ����������й�������ŵ����2020�꣬��λGDP������̼�ŷű�2005���½�40%��50%��
������CO2Ũ�ȵij����߸��Ѿ��������ǵĸ߶����ӣ���ѧ����ָ�������ж�����̼�ij�������������ʹȫ���ů�������ȫ�ı��ź�ˮ���ܽ����̼��CO2��HCO3-��CO32-����Ũ����������й�������ŵ����2020�꣬��λGDP������̼�ŷű�2005���½�40%��50%��| 1 |
| 2 |
| 3 |
| 2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
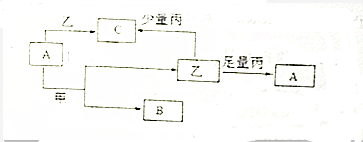
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| A���õ����Zn��������������ԭ��Ӧ |
| B���õ�ط�Ӧ��MnO2������� |
| C���õ�ع���ʱ������Zn����������MnO2 |
| D���õ��������ӦʽΪ��MnO2+e-+H2O=MnOOH+OH- |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
| �� | �� | �� | |
| A | Al2O3 | HNO3 | Ba��OH��2 |
| B | NH3 | O2 | H2SO4 |
| C | SiO2 | NaOH | HF |
| D | CO2 | Na2O2 | H2O |
| A��A | B��B | C��C | D��D |
�鿴�𰸺ͽ���>>
����ѧУ��ѡ - ��ϰ���б� - �����б�
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com